题目内容
14.人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则使血红蛋白中Fe2+转化为Fe3+丧失其生理功能,临床证明服用维生素C可以解毒.下列叙述正确的是( )| A. | 中毒反应中亚硝酸盐是氧化剂 | |
| B. | 维生素C能将Fe3+氧化为Fe2+,使其解毒 | |
| C. | 中毒反应中Fe3+是还原产物 | |
| D. | 维生素C能将亚硝酸盐氧化成硝酸盐,使其解毒 |
分析 Fe2+转化为Fe3+,铁元素发生了氧化反应,须加入氧化剂实现,Fe3+转化为Fe2+,铁元素发生了氧化反应,须加入还原剂实现.
解答 解:A、根据题意亚硝酸盐使血红蛋白中的Fe2+转化为高铁Fe3+,所以亚硝酸盐是氧化剂,故A正确;
B、维生素C具有还原性,可使Fe3+还原为Fe2+,故B错误;
C、中毒反应中Fe3+是氧化产物,故C错误;
D、维C可使Fe3+转化为Fe2+,让铁元素发生氧化反应,故D错误.
故选A.
点评 本题考查学生氧化还原反应,明确基本概念知识和元素的化合价变化,结合信息来解答,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
4.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O═C6H5OH+HSO3- | |
| C. | 向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
5.利用下列实验装置能完成相应实验的是( )
| A. |  用于证明非金属性强弱:Cl>C>Si | B. | 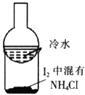 用于分离I2和NH4Cl | ||
| C. |  装置能组成Zn、Cu原电池 | D. |  用于测定某稀盐酸的物质的量浓度 |
2.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(OH-)相等 | |
| B. | 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 常温下物质的量浓度相等的①NH4HCO3、②NH4HSO4、③NH4Fe(SO4)2:三种溶液中NH4+的浓度:②>③>① | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数:N前>N后 |
9.下列关于化学的描述中,不正确的是( )
| A. | 化学是一门具有创造性和实用性的科学 | |
| B. | 人们可以利用先进的技术和设备在化学反应中制造出新原子和新分子 | |
| C. | 制陶、冶金及酿酒过程中,肯定发生了化学变化 | |
| D. | 化学家可以在微观层面上操纵分子和原子,组装分子器件和分子机器等 |
4.下列叙述正确的是( )
| A. | 摩尔是国际单位制的7个基本物理量之一 | |
| B. | 物质的量可以理解为物质的质量 | |
| C. | 物质的量的单位是“摩尔” | |
| D. | 物质的量是表示物质的数量的单位 |
 实验室用如图所示装置验证苯与溴反应的产物以及反应类型.
实验室用如图所示装置验证苯与溴反应的产物以及反应类型. +Br2
+Br2 
 +HBr;
+HBr;