题目内容
右图各个装置中能组成原电池的是: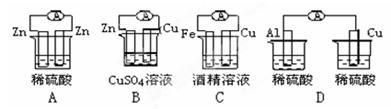
B
解析试题分析:A、两电极的活泼性相同,所以不能构成原电池,错误;B、符合原电池的构成条件,所以能构成原电池,正确;C、酒精是非电解质,该装置不能自发的进行氧化还原反应,所以不能构成原电池,错误;D、该装置不能形成闭合回路,所以不能构成原电池,错误。
考点:本题考查原电池的构成条件。

练习册系列答案
相关题目
氢氧燃料电池是一种新能源。下图为氢氧燃料电池示意图。下列说法不正确的是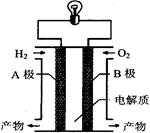
| A.电子由B极通过导线流向A极 |
| B.A极是负极,B极是正极 |
| C.该装置能将化学能转化为电能 |
| D.产物为无污染的水,属于环境友好电池 |
如图所示,下列叙述中正确的是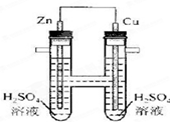
| A.正极发生氧化反应 | B.电子通过导线由铜流向锌 |
| C.负极有O2逸出 | D.铜上有H2逸出 |
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱。 |
| D.电池正极的电极反应为4H++O2+4e-=2H2O |
下列事实与电化学腐蚀无关的是
| A.生铁比纯铁易生锈 |
| B.黄铜(铜锌合金)制品不易产生铜绿 |
| C.纯银饰品久置表面变暗 |
| D.与铜管连接的铁管易生锈 |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是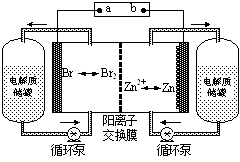
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
| A.铜片、铁片、FeCl3溶液组成的原电池 |
| B.石墨、铁片、Fe(NO3)3溶液组成的原电池 |
| C.铁片、锌片、Fe2(SO4)3溶液组成的原电池 |
| D.铜片、铁片、Fe(NO3)3溶液组成的原电池 |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法正确的是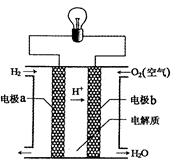
| A.该电池工作时电能转化为化学能 |
| B.通入氢气的一极是负极 |
| C.外电路中电子由电极b通过导线流向电极a |
| D.该电池的总反应:2H2+O2=2H2O |
将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转。下列针对该装置的说法正确的是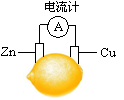
| A.将电能转化为化学能 |
| B.电子由铜片流出 |
| C.锌片是负极. |
| D.铜片逐渐被腐蚀 |