题目内容
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
名称 | 苯 | 溴 | 溴苯 |
密度/(g·cm-3) | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
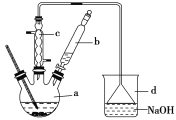
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置d的作用是___________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是___________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须用到的是________(填字母序号)。
a.重结晶b.过滤c.蒸馏d.萃取
【答案】HBr 防倒吸,吸收HBr、溴蒸气 除去Br2、HBr 吸收水分 ![]() C
C
【解析】
本实验的目的是合成溴苯,在a(三颈烧瓶)中加入15mL无水苯和少量铁屑,在b(分液漏斗)中小心加入4.0mL液态溴,之后向a中滴入几滴溴,溴与Fe反应生成FeBr3,在FeBr3的催化作用下苯和溴发生取代反应生成溴苯和HBr气体,HBr气体遇到空气中的水蒸气凝结成小液滴,产生白雾;装置c(球形冷凝管)可以冷凝回流溴和苯,提高利用率,装置d可以吸收尾气,倒置漏斗可以防止倒吸;反应完成后对产物进行提纯:加水溶解水溶性杂质,过滤除去铁屑,再用水洗去部分杂质,溴在水中溶解度较小,之后用10%的NaOH溶液洗去残留的Br2和HBr,然后再用水洗去NaOH,分液分离,再经无水氯化钙干燥,静置过滤得到粗产品,此时剩余的杂质为与溴苯互溶的苯,二者沸点差异较大,可蒸馏除去。
(1)在溴化铁作催化剂条件下,苯和溴发生取代反应生成溴苯和HBr,HBr遇水蒸气产生白雾,所以产生白雾的是因为生产的HBr;HBr、Br2蒸气会污染空气,可用碱液吸收,所以d的作用是吸收HBr和Br2,同时倒置漏斗可以防止倒吸;
(2)②NaOH溶液可以洗去溴苯表面的残留的Br2和HBr;
③分出的粗苯表面有一定水分,加入无水氯化钙可以吸收水分;
(3)经以上分离操作后,粗溴苯中还有与其互溶的苯(![]() )杂质,根据表格数据可知二者沸点差异较大,可蒸馏除去,所以选C。
)杂质,根据表格数据可知二者沸点差异较大,可蒸馏除去,所以选C。

【题目】相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ: |
② | 0 | 0 | 2 | 吸收热量:Q |
实验还测得到达平衡后,两容器中相同组分的质量分数(或体积分数)都相同。下列叙述正确的是( )
A.容器①、②中反应的平衡常数不相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.平衡时,两个容器中反应物的转化率之和等于1
D.容器②中达平衡时吸收的热量Q=23.15kJ