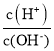题目内容
【题目】设NA为阿伏加德罗常数值。下列有关叙述不正确的是
A.浓硝酸热分解生成NO2、N2O4共23g,转移电子数为0.5NA
B.10g46%乙醇水溶液中所含氧原子数为0.4NA
C.1L1mol/LNa2CO3溶液中,阴离子总数小于NA
D.向100mL0.1mol/L醋酸溶液中加入CH3COONa固体至溶液刚好为中性,溶液中醋酸分子数为0.01NA
【答案】C
【解析】
A. 假设23g全部是NO2,转移电子物质的量为![]() =0.5mol,假设全部是N2O4,转移电子物质的量为
=0.5mol,假设全部是N2O4,转移电子物质的量为![]() =0.5mol,因此生成23g该混合物时,转移电子物质的量为0.5mol,故A说法正确;
=0.5mol,因此生成23g该混合物时,转移电子物质的量为0.5mol,故A说法正确;
B. 乙醇水溶液中含氧物质有CH3CH2OH和H2O,因此10g46%乙醇水溶液中所含氧原子物质的量为(![]() )=0.4mol,故B说法正确;
)=0.4mol,故B说法正确;
C. Na2CO3属于强碱弱酸盐,CO32-发生水解:CO32-+H2O ![]() HCO3-+OH-,溶液中阴离子物质的量大于1L×1mol·L-1=1mol,故C说法错误;
HCO3-+OH-,溶液中阴离子物质的量大于1L×1mol·L-1=1mol,故C说法错误;
D. 根据电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),因为溶液显中性,因此有c(Na+) =c(CH3COO-),根据物料守恒,因此有c(CH3COO-)+c(CH3COOH)=0.1mol·L-1+c(Na+),两式联立得出:c(CH3COOH)=0.1mol·L-1,即该溶液中醋酸分子物质的量为0.01mol,故D说法正确;
答案:C。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液。称量时,样品可放在___(填字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定时,用0.2000mol·L-1的盐酸来滴定待测溶液,不可选用__(填字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中,眼睛应注视___。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是__mol·L-1,烧碱样品的纯度是___(保留两位数字)。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果___。
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果___。