题目内容
【题目】克伦特罗是一种平喘药,但被违法添加在饲料中,俗称“瘦肉精”,其结构简式如图。下列有关“瘦肉精”的说法正确的是

A. 它的分子式为C12H17N2Cl2O
B. 它含有氨基、氯原子、碳碳双键等官能团
C. 1mol克伦特罗最多能和3 molH2发生加成反应
D. 一定条件下它能发生水解反应、酯化反应、消去反应、氧化反应、加聚反应等
【答案】C
【解析】
试题A、根据克伦特罗结构简式知它的分子式为C12H18N2Cl2O,错误;B、根据克伦特罗结构简式知它含有苯环、氨基、氯原子、羟基等官能团,不含碳碳双键,错误;C、该有机物含有1个苯环,1mol克伦特罗最多能和3 molH2发生加成反应,正确;D、该有机物不能发生加聚反应,错误。

 口算能手系列答案
口算能手系列答案【题目】下列实验过程不能达到实验目的的是
编号 | 实验目的 | 实验过程 |
A | 探究浓度对平衡的影响 | 各取2mL0.1mol/L的重铬酸钾溶液于两支试管中,分别加入5~15滴浓硫酸和5~15滴6mol/L氢氧化钠溶液, 记录溶液颜色的变化 |
B | 探究温度对平衡的影响 | 将两份等浓度含有少量酚酞的氨水分别置于冰水浴和40℃热水浴中(忽略NH3的挥发),记录溶液颜色的 变化 |
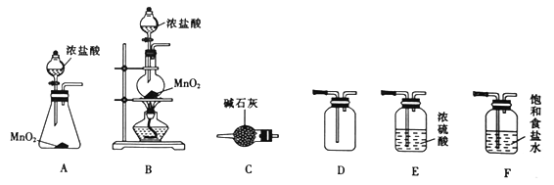
C | 制取并纯化氯气 | 向高锰酸钾固体中滴加浓盐酸,将产生的气体依次通过饱和食盐水、浓硫酸的洗气瓶 |
D | 证明催化效果Fe3+>Cu2+ | 向2支盛有2 mL相同温度,相同浓度H2O2溶液的试管中同时加入5滴氯化铁溶液和硫酸铜溶液,观察实验现象 |
A. A B. B C. C D. D
【题目】利用水钴矿[主要成分为Co2O3和Co(OH)3,还有少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如图所示:
 已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式__________________________。
(2)NaClO3的作用是___________________________________。
(3)加Na2CO3调pH至5.2所得沉淀为____________________________。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。萃取剂的作用是_____;其使用的适宜pH范围是_____(填字母)。

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取w g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取25.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取25.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。(5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O)
滴定次数实验数据 | 1 | 2 | 3 | 4 |
待测溶液体积/mL | 25.00 | 25.00 | 25.00 | 25.00 |
滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
滴定管末读数/mL | 19.95 | 20.20 | 19.15 | 20.20 |
实验中所记录的数据如下表:
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、胶头滴管、量筒、药匙和_________、____________。
(2)操作I为________操作Ⅱ为____________
(3)方案I中如何判断加入的氯化钡已经过量_____________,在方案Ⅱ中滴定终点的判断方法是________________。
(4)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为_________。
(5)上述实验中,由于操作错误所引起的误差分析正确的是_________
A.方案I中若没有洗涤操作,实验结果将偏小
B.方案I中若没有操作Ⅱ,实验结果将偏大
C.方案Ⅱ中,滴定管在滴定前无气泡,滴定后出现气泡,实验结果偏小
D.方案Ⅱ中,滴定终点时仰视读数,实验结果偏大