题目内容
【题目】

①配制一定物质的量浓度的硬脂酸的苯溶液;
②测定从胶头滴管滴出的每滴液体的体积;
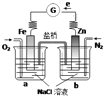
③测定在水槽水面上形成硬脂酸单分子膜所需硬脂酸苯溶液的滴数,(如上图所示)用胶头滴管
吸取硬脂酸的苯溶液,垂直往水面中滴一滴,待苯在水面上全部挥发,硬脂酸分子在水面扩散至看不到油珠时,再滴第二滴,如此逐滴滴下,直到整个水面形成单个分子厚的硬脂酸分子所形成的膜为止(该单分子膜分子是紧密排列的,此时如再滴入硬脂酸溶液,该溶液在水面上不再扩散);
④测量水槽中水的表面积;
⑤计算求得阿伏加德罗常数。
(1)在第一步实验中,称取一定质量的硬脂酸后,配制溶液所需的玻璃仪器主要有 、 、 。
(2)第二步实验,测定从胶头滴管滴出的每滴液体的体积,常用方法是
(3)若硬脂酸苯溶液的浓度为c molL-1,测得胶头滴管滴出的每滴溶液的体积为V mL,水面上形成硬脂酸单分子膜时滴下的硬脂酸溶液的滴数为d,水槽中水的表面积为S cm2,每个硬脂酸分子的截面积为A cm2。求阿伏加德罗常数NA(用c、V、d、S、A的代数式表示): 。
(4)若水中含有少量氢氧化钠溶液,则会对测定的NA值有何影响? (选填“偏大”、“偏小”或“无影响”)。
【答案】(1)容量瓶、烧杯、胶头滴管、玻璃棒;
(2)往小量筒中滴入1 mL溶液,然后记下总滴数,从而计算出1滴溶液的体积;
(3)NA=1000S/AcdV;
(4)偏小。
【解析】试题分析:(1)配制一定物质的量浓度的实验,需要的步骤是:称量→溶解→冷却→转移→洗涤→振荡→定容→摇匀,称取一定质量的硬脂酸钠后,需要的仪器有烧杯、玻璃棒、容量瓶、胶头滴管;(2)就像初中学过,一张纸的质量不容易测,但可以测出50张纸的质量,然后除以总张数,就是一张纸的质量,因此往小量筒中滴入1 mL溶液,然后记下总滴数,从而计算出1滴溶液的体积;(3)水面上形成硬脂酸单分子膜需要的硬脂酸苯溶液的体积为VdmL,需要硬脂酸的物质的量为Vd×10-3×cmol,水槽中水的表面积等于所有硬脂酸分子的截面积,即Vd×10-3×c×NA×A=S,则NA=1000S/AcdV;(4)含有少量的NaOH,硬脂酸与NaOH发生反应,需要的硬脂酸的体积增大,根据上述阿伏加德罗常数的公式,NA将会偏小。