题目内容
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
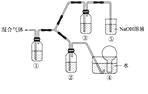
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
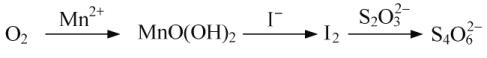
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式;_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(用mg·L1表示),写出计算过程。
【答案】(3)①O2+2Mn2++4OH-=MnO(OH)2↓
②在100.00mL水样中
I2+2S2O32-=2I-+S4O62-
n(I2)=![]()
=![]()
=6.750×10-5mol
n[MnO(OH)2]= n(I2)= 6.750×10-5mol
n(O2)= ![]() n[MnO(OH)2]=
n[MnO(OH)2]=![]() ×6.750×10-5mol=3.375×10-5mol
×6.750×10-5mol=3.375×10-5mol
水中溶解氧=![]() =10.80mg/L
=10.80mg/L
【解析】
试题分析:
(3)①O2将Mn2+氧化成MnO(OH)2中氧气是氧化剂,得到4个电子,Mn元素的化合价从+2价升高到+4价,失去2个电子,所以根据电子得失守恒以及原子守恒可知反应的离子方程式为O2+2Mn2++4OH-=MnO(OH)2↓。
②根据流程图并依据电子得失守恒可知氧气得到的电子就是硫代硫酸钠失去的电子,在反应中S元素化合价从+2价升高到+2.5价,1mol硫代硫酸钠失去1mol电子,一分子氧气得到4个电子,所以根据电子得失守恒可知该水样中的溶解氧为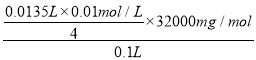 =10.80mg/L。
=10.80mg/L。

 考前必练系列答案
考前必练系列答案