题目内容
【题目】图1是部分短周期元素的常见化合价与原子序数的关系图: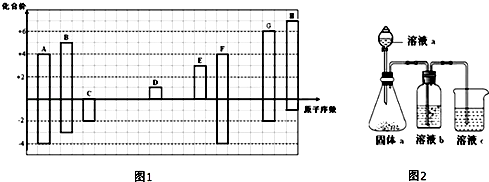
(1)元素F在周期表中的位置 .
(2)DH其所含化学键类型为 .
(3)C、D、G对应的简单离子半径大小顺序是 . (用离子符号回答)
(4)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:①溶液a和溶液b分别为 , .
②溶液c中的离子反应方程式为 .
【答案】
(1)第三周期ⅣA族
(2)离子键
(3)S2﹣>O2﹣>Na+
(4)硝酸;饱和NaHCO3溶液;SiO ![]() +CO2+H2O=H2SiO3↓+CO
+CO2+H2O=H2SiO3↓+CO ![]() 或SiO
或SiO ![]() +2CO2+2H2O=H2SiO3↓+2HCO
+2CO2+2H2O=H2SiO3↓+2HCO ![]()
【解析】解:短周期元素中,A、F均有+4、﹣4价,处于ⅣA族,且原子序数A<F,故A为碳、F为Si;C、G均有﹣2价,且G有+6,G的原子序数较大,故C为O元素、G为S元素;B有+5、﹣3价,原子序数介于碳、氧之间,故B为N元素;H有+7、﹣1价,原子序数大于硫,则H为Cl;D有+1价,E有+3价,分别处于ⅠA族、ⅢA族,原子序数氧<D<E<Si,故D为Na,E为Al.(1)元素F为Si,在周期表中的位置:第三周期ⅣA族,所以答案是:第三周期ⅣA族;(2)DH为NaCl,其所含化学键类型为离子键,所以答案是:离子键;(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越小,简单离子半径大小顺序是:S2﹣>O2﹣>Na+ , 所以答案是:S2﹣>O2﹣>Na+;(4)利用最高价含氧酸的酸性强弱,证明A、B、F的非金属性强弱关系,溶液a为硝酸,溶液b为饱和NaHCO3溶液,溶液c为硅酸钠溶液,溶液c中的离子反应方程式为:SiO ![]() +CO2+H2O=H2SiO3↓+CO
+CO2+H2O=H2SiO3↓+CO ![]() 或SiO
或SiO ![]() +2CO2+2H2O=H2SiO3↓+2HCO
+2CO2+2H2O=H2SiO3↓+2HCO ![]() ,所以答案是:①硝酸;饱和NaHCO3溶液;②SiO
,所以答案是:①硝酸;饱和NaHCO3溶液;②SiO ![]() +CO2+H2O=H2SiO3↓+CO
+CO2+H2O=H2SiO3↓+CO ![]() 或SiO
或SiO ![]() +2CO2+2H2O=H2SiO3↓+2HCO
+2CO2+2H2O=H2SiO3↓+2HCO ![]() .
.

 优百分课时互动系列答案
优百分课时互动系列答案【题目】某同学用15molL﹣1浓硫酸,按下列步骤配2505mL0.1molL﹣1H2SO4溶液,请回答有关问题.
(1)完成下列表格:
实验步骤 | 有关问题 |
①计算所需浓硫酸的体积 | 需取浓硫酸()mL |
②量 取浓硫酸 | 需要用到的主要仪器是: |
③将 浓硫酸并搅拌 | 该操作要做到胆大心细,杜绝事故发生 |
④待溶液冷却至室温,将烧杯中溶液转移至 mL容量瓶中 | 要注意把洗涤液一并转移至容量瓶中 |
⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1﹣2cm处后的正确操作是: |
(2)本实验不需要用到的仪器是
a.玻璃棒 b.烧杯 c.天平 d胶头滴管
(3)在进行④步操作时,不慎将溶液溅到容量瓶外,则配制溶液的浓度将(填写偏高、偏低、不影响.下同).若配制时容量瓶没有干燥,则配制溶液浓度将 .
(4)某研究人员应用如图研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸汽.请回答下列问题: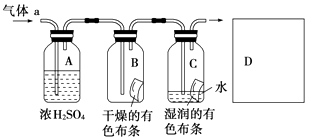
①浓硫酸的作用是 .
②通入Cl2后,从集气瓶B中干燥的有色布条的现象可得出的结论是从集气瓶C中湿润的有色布条的现象可得出的结论是 .
③从物质性质的方面来看,这样的实验设计还存在事故隐患,请在图D处以图的形式表明克服事故隐患的措施.