题目内容
【题目】在下面的横线上填上适当的内容。
(1)![]() 个Na+约含__________mol Na+,其质量为______________g。
个Na+约含__________mol Na+,其质量为______________g。
(2)4.5molCH4约含有___________个CH4,其质量为____________g。
(3)![]() 个SO42-约含________mol SO42-,其质量为___________g;49g H2SO4 约含有______个H,共含有___________个原子。
个SO42-约含________mol SO42-,其质量为___________g;49g H2SO4 约含有______个H,共含有___________个原子。
【答案】10 230 ![]() 72 0.5 48
72 0.5 48 ![]()
![]()
【解析】
1.![]() 个Na+的物质的量为
个Na+的物质的量为![]() ,对应的质量为
,对应的质量为![]() ,故答案为:10;230;
,故答案为:10;230;
2.4.5mol CH4的个数为![]() ,其质量为
,其质量为![]() ,故答案为:
,故答案为:![]() ;72;
;72;
3.![]() 个SO42的物质的量为
个SO42的物质的量为![]() ,质量为,48g H2SO4含有的分子的个数
,质量为,48g H2SO4含有的分子的个数![]() ,含有的原子数为
,含有的原子数为![]() ,故答案为:0.5;48;
,故答案为:0.5;48;![]() ;
;![]() 。
。

练习册系列答案
相关题目
【题目】元素周期表是学习化学的重要工具,它隐含许多信息和规律。
(1)下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 |
|
| 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)用元素代号标出它们在周期表中对应位置__________(以下为周期表的一部分)
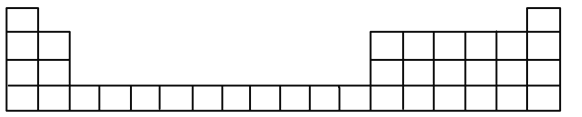
(2)![]() 元素处于周期表中______周期______族
元素处于周期表中______周期______族
(3)在元素周期表中______的分界处,可以找到制半导体材料的元素
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是______(填化学式)
(5)C、E形成化合物为______(填化学式)