题目内容
8.电解原理在化学工业中有广泛应用.(1)图1是电解食盐水的工业模拟图
①电解饱和食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑
②溶液A是氢氧化钠浓溶液
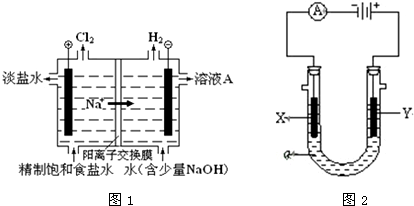
(2)图2是实验室常用的电解池装置,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X(填X或Y)极附近观察溶液变红.
②Y电极上的电极反应式为2Cl--2e-=Cl2↑,检验该电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是纯铜,电极反应式是Cu2++2e-=Cu.
分析 (1)①用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时溶液中生成氢氧化钠,据此书写离子;
②用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时溶液中生成氢氧化钠;
(2)①用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极X电极上氢离子放电生成氢气,同时溶液中生成氢氧化钠,滴加酚酞,溶液变红;
②用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,氯气具有氧化性,可以用湿润的碘化钾淀粉试纸检验;
(3)电解方法精炼粗铜,电解液是含有铜离子的盐溶液,阴极的材料是纯铜,阳极材料是粗铜,据此回答.
解答 解:(1)①用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时溶液中生成氢氧化钠,所以电池反应式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,电解饱和食盐水的离子方程式为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
②用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时溶液中生成氢氧化钠,即溶液A是氢氧化钠浓溶液;故答案为:氢氧化钠浓溶液;
(2)①用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极X电极上氢离子放电生成氢气,同时溶液中生成氢氧化钠,滴加酚酞,所以X极溶液变红,故答案为:X;
②用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气,电极反应为:2Cl--2e-=Cl2↑,氯气的检验方法:把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色,故答案为:2Cl--2e-=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;
(3)电解方法精炼粗铜,电解液是含有铜离子的盐溶液,如CuSO4溶液,则阴极的材料是纯铜,阳极材料是粗铜,在阴极区域发生反应:Cu2++2e-=Cu,故答案为:纯铜;Cu2++2e-=Cu.
点评 本题考查了电解原理、气体的检验等知识点,明确离子放电顺序是解本题关键,氯气可以用淀粉碘化钾检验,难度不大.

| A. | 0.5 mol•L-1 | B. | l mol•L-1 | C. | 2 mol•L-1 | D. | 3 mol•L-1 |
| A. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| B. | 氯离子(Cl-)的结构示意图: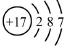 | |
| C. | 氯分子的电子式:${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$ | |
| D. | 氯乙烯分子的结构简式:H3C-CH2Cl |
| 选项 | 目的 | 操作 |
| A | 配制100 mL 1.0 mol/L CuSO4溶液 | 将25 g CuSO4•5H20溶于100 mL蒸馏水中 |
| B | 除去KNO3中少量NaCl | 将混合物制成热的浓溶液,冷却结晶,过滤、洗涤 |
| C | 检验某溶液中是否含硫酸根 | 向溶液中先加盐酸后加氯化钡 |
| D | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
| A. | A | B. | B | C. | C | D. | D |
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
| A. | 反应开始时,反应速率:甲<乙<丙 | |
| B. | 平衡时,甲中和丙中H2的转化率均是60% | |
| C. | 平衡时,c(CO2)丙=2c(CO2)甲 | |
| D. | 平衡时,乙中CO2的体积分数大于60% |
| X的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y元素的族序数是周期序数的三倍 |
| Z元素的电负性在所有元素中最大 |
| W原子的第一至第六电离能分别为:I1=578KJ•mol-1,I2=1817KJ•mol-1,I3=2745KJ•mol-1,I4=11575KJ•mol-1,I5=14830KJ•mol-1,I6=18376KJ•mol-1 |
| Q为前四周期中电负性最小的元素 |
| R原子最高能层上只有1个单电子,其余各能层均已充满电子. |
(1)R在周期表中位于ds区,写出R基态原子的价电子排布式3d104s1.
(2)X与Y形成的二元化合物中属于非极性分子的CO2 (用化学式表示).
(3)写出Z元素的单质与水反应的方式2F2+2H2O=4HF+O2,此反应中氧化剂与氧化产物物质的量之比为2:1.
(4)X的氯化物的熔点比Q的氯化物的熔点低(“高”或“低”),理由是CCl4属于分子晶体,KCl属于离子晶体.
(5)光谱证实单质W与强碱性溶液反应有[W(OH)4]-生成,则中[W(OH)4]--存在acd(填选项字母)
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
(6)金刚砂(SiC)的结构与金刚石(4个碳原子在立方体体内,其余碳原子分别位于面心和顶角)相似,硬度与金刚石相当,则金刚砂的晶胞中含有4个硅原子,4个碳原子,其中硅原子的杂化方式为sp3.
| A. | 原裂纹处有碳积存 | |
| B. | 裂纹处表面积很大,反应快 | |
| C. | 裂纹处的尘埃起催化作用 | |
| D. | 裂纹处有氧化铁积存,并与盐酸作用生成可溶性氯化物 |
| 一个分子 | 含有原子的种类及其数目 | 原子总数 | 质子总数 |
| O2 | |||
| H2O | |||
| NH3 | |||
| H2SO4 |