题目内容
【题目】在标准状况下有一定量的气体如下:①6.72LCH4、②3.01×1023个HCl分子、③13.6gH2S、④0.2molNH3,下列对这四种气体的关系从大到小排列的组合中正确的是( )
a.体积:②>③>①>④ b.密度:②>③>④>①
c.质量:②>③>①>④ d.氢原子个数:①>③>④>②
A.abcB.bcdC.abcD.abcd
【答案】D
【解析】
标况下,气体摩尔体积相等,①6.72L CH4的物质的量n(CH4)=![]() =0.3mol,②3.01×1023个HCl分子的物质的量n(HCl)=
=0.3mol,②3.01×1023个HCl分子的物质的量n(HCl)=![]() =0.5mol;③13.6g H2S的物质的量n(H2S)=
=0.5mol;③13.6g H2S的物质的量n(H2S)=![]() =0.4mol、④0.2mol NH3。
=0.4mol、④0.2mol NH3。
a.V=n·Vm知,相同条件下,气体体积与物质的量成正比,所以这几种气体体积大小顺序是:②>③>①>④,a正确;
b.根据ρ=![]() 可知:气体密度与摩尔质量成正比,甲烷摩尔质量是16g/mol、HCl摩尔质量是36.5g/mol、H2S摩尔质量是34g/mol、NH3摩尔质量是17g/mol,所以气体密度大小顺序是:②>③>④>①,b正确;
可知:气体密度与摩尔质量成正比,甲烷摩尔质量是16g/mol、HCl摩尔质量是36.5g/mol、H2S摩尔质量是34g/mol、NH3摩尔质量是17g/mol,所以气体密度大小顺序是:②>③>④>①,b正确;
c.甲烷的质量m(CH4)=0.3mol×16g/mol=4.8g,HCl的质量m(HCl)=0.5mol×36.5g/mol=18.25g,H2S的质量m(H2S)=13.6g、氨气的质量m(NH3)=0.2mol×17g/mol=3.4g,所以质量大小顺序是:②>③>①>④,c正确;
d.根据N=n·NA知,气体分子数之比等于其物质的量之比,结合分子构成知,甲烷分子中H原子物质的量=0.3mol×4=1.2mol,HCl中H原子的物质的量等于HCl分子的物质的量为0.5mol,H2S中H原子的物质的量=0.4mol×2=0.8mol,NH3分子中H原子的物质的量=0.2mol×3=0.6mol,所以H原子个数大小顺序是:①>③>④>②,d正确;
故合理选项是D。

【题目】工业上以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为:Na2Cr2O7·2H2O),其主要工艺流程如下:

查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42—,自身被还原为Bi(OH)3固体。
ii.
物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 | Bi(OH)3 |
开始沉淀的PH | 2.7 | 3.4 | 4.6 | 7.5 | 0.7 |
完全沉淀的PH | 3.7 | 4.4 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)将铬铁矿矿石粉碎的目的是___________。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和___________(填仪器名称)。
(3)写出④反应的化学方程式________________。
(4)⑤中酸化是使CrO42—转化为Cr2O72—。写出该反应的离子方程式______。
(5)将溶液H经下列操作:蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
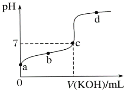
(6)取一定质量的固体D溶解于200mL的稀硫酸中,向所得溶液中加入5.0mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为_________,固体D中含Fe化合物的物质的量为___________。