题目内容
11.短周期主族元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.Z原子的最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍.X与Y、Z位于相邻的周期.下列说法正确的是( )| A. | X的最高价氧化物对应的水化物是弱酸 | |
| B. | Z位于元素周期表的第3周期第ⅥA族 | |
| C. | Y的最高氧化物对应的水化物能溶于NaOH溶液 | |
| D. | 原子半径的大小顺序:r(Z)>r(Y)>r(X) |
分析 短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍,最外层电子数不超过8个,K层不超过2个,则X内层电子数是2,所以X位于第二周期,Y、Z位于第三周期,则Z为S元素,Y最外层电子数为2,且处于第三周期,为Mg元素,这三种元素原子的最外层电子数之和为13,Y、Z最外层电子数之和为8,所以X最外层电子数为5,故X为N元素,据此解答.
解答 解:短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍,最外层电子数不超过8个,K层不超过2个,则X内层电子数是2,所以X位于第二周期,Y、Z位于第三周期,则Z为S元素,Y最外层电子数为2,且处于第三周期,为Mg元素,这三种元素原子的最外层电子数之和为13,Y、Z最外层电子数之和为8,所以X最外层电子数为5,故X为N元素.
A.X的最高价氧化物对应的水化物为硝酸,属于强酸,故A错误;
B.Z为S元素,位于元素周期表的第3周期ⅥA族,故B正确;
C.氢氧化镁不能溶于氢氧化钠溶液,故C错误;
D.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径r(Mg)>r(S)>r(N),故D错误,
故选B.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,需要学生熟练掌握核外电子排布,侧重考查分析、推断能力,难度中等.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
2.下列离子方程式正确的是( )
| A. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 澄清石灰水跟盐酸反应:H++OH-═H2O | |
| C. | 在硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙中加入盐酸:CO32-+2H+═CO2↑+H2O |
19.如表中对应关系错误的是( )
| A | NaCl═Na++Cl NH3•H2O?NH4++OH- | 均属于电离方程式 |
| B | 向溶液中滴加盐酸酸化过的BaCl2溶液,出现白色沉淀 | 说明该溶液中一定有SO${\;}_{4}^{2-}$ |
| C | Ba2++SO${\;}_{4}^{2-}$═BaSO4↓; HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O | 均可表示一类反应 |
| D | Cl2+2NaOH═NaCl+NaClO+H2O; 3S+6NaOH═2Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
| A. | A | B. | B | C. | C | D. | D |
6.某小组同学利用铝和氧化铁发生铝热反应后得到的固体进行如表实验.
(1)铝和氧化铁反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
(2)固体成分的初步确定.
①由上述实验可知:i所得溶液中Fe元素的存在形式有Fe2+、Fe3+;
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含A1单质,设计了相关实验,依据的原理是(用离子方程式表示)2Al+2OH-+2H2O=2AlO2-+3H2↑;
③生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(3)该小组同学对ii中溶液红色褪去的原因做进一步探究.
提示:KSCN中S元素的化合价为-2价
①实验iii中白色沉淀的化学式是BaSO4;
②结合实验iii和iv分析,实验ii中红色褪去的原因是溶液中SCN-离子被H2O2氧化,溶液红色褪去.
| 实验序号 | 操作及现象 |
| ⅰ | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ⅱ | 向ⅰ中所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液至过量,产生无色气体(经检验为O2),溶液变为深红色,且红色很快褪去 |
(2)固体成分的初步确定.
①由上述实验可知:i所得溶液中Fe元素的存在形式有Fe2+、Fe3+;
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含A1单质,设计了相关实验,依据的原理是(用离子方程式表示)2Al+2OH-+2H2O=2AlO2-+3H2↑;
③生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(3)该小组同学对ii中溶液红色褪去的原因做进一步探究.
| 实验序号 | 操作及现象 |
| ⅲ | 将ⅱ中剩余溶液均分为两份,一份滴加NaOH溶液,产生红褐色沉淀; 另一份滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀不溶解 |
| ⅳ | 取2mL 0.1mol•L-1 FeCl3溶液,滴入KSCN溶液,溶液变为红色,通入一段时间O2,无明显变化.再加入H2O2溶液,红色很快褪去 |
①实验iii中白色沉淀的化学式是BaSO4;
②结合实验iii和iv分析,实验ii中红色褪去的原因是溶液中SCN-离子被H2O2氧化,溶液红色褪去.
16.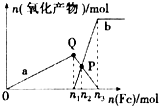 含1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )
含1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )
 含1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )
含1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )| A. | 曲线a表示Fe2+,曲线b表示Fe3+ | |
| B. | P点时总反应的离子方程式可表示为5Fe+16H++NO3-═3Fe2++2Fe3++4NO↑+8H2O | |
| C. | n2=0.25 | |
| D. | n3:n1=3:2 |
3.下列反应中,反应后固体物质质量增加的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 漂白粉久置后变质 | D. | Fe(OH)2在空气中灼烧 |
20.某化学反应2A(g)?B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况如表:
根据表中数据,完成下列填空:
(1)实验1,反应在10至20分钟时间内A平均速率为0.013mol/(L.min).
(2)实验2,A的初始浓度c2=1.0 mol•L-1,推测实验2中还隐含的条件是加入催化剂.
(3)800℃时该反应的平衡常数K=0.25
(4)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、<、=),且C3=1.2mol•L-1.
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)实验1,反应在10至20分钟时间内A平均速率为0.013mol/(L.min).
(2)实验2,A的初始浓度c2=1.0 mol•L-1,推测实验2中还隐含的条件是加入催化剂.
(3)800℃时该反应的平衡常数K=0.25
(4)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、<、=),且C3=1.2mol•L-1.
1.2011年“世界地球日”的主题是“珍惜地球资源,转变发展方式”.下列做法可行的是( )
| A. | 用土填埋废弃塑料,防止白色污染 | |
| B. | 使用车乙醇汽油,防止温室效应 | |
| C. | 化工厂加高烟囱排放废气,防止酸雨 | |
| D. | 废旧电池中汞的回收可减少对环境的污染 |
 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1的硫酸溶液进行中和热的测定,实验装置如图所示:
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1的硫酸溶液进行中和热的测定,实验装置如图所示: