题目内容
(10分)味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”。某学校化学科研小组现对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验试剂:水、试剂X的溶液等
(2)实验过程:
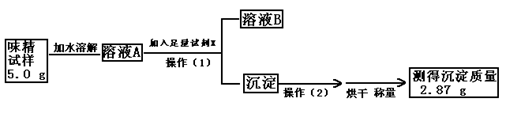 [
[
根据上述实验步骤回答下列有关问题:
①试剂X是 ,其作用是 。
②操作(1)所需要的玻璃仪器有 。
③操作(2)的名称 是 。
是 。
④通过计算判断该味精中NaCl的质量分数,是否符合其包装上标注的标准 。
⑤如果溶液A为50 mL,则溶液A中NaCl的物质的量浓度是多少?
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验试剂:水、试剂X的溶液等
(2)实验过程:
 [
[根据上述实验步骤回答下列有关问题:
①试剂X是 ,其作用是 。
②操作(1)所需要的玻璃仪器有 。
③操作(2)的名称
 是 。
是 。④通过计算判断该味精中NaCl的质量分数,是否符合其包装上标注的标准 。
⑤如果溶液A为50 mL,则溶液A中NaCl的物质的量浓度是多少?
(10分)① AgNO3溶液(1分) 沉淀NaCl中的Cl-(1分)
②普通漏斗烧杯玻璃棒(3分)
③ 洗涤(1分)
④不符合(2分)
⑤0.4mol/L(2分)
②普通漏斗烧杯玻璃棒(3分)
③ 洗涤(1分)
④不符合(2分)
⑤0.4mol/L(2分)
略

练习册系列答案
相关题目
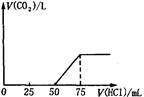
 CO3和KHCO3的混合物4.60 g,与1.00 mol/L的盐酸反应.
CO3和KHCO3的混合物4.60 g,与1.00 mol/L的盐酸反应. 2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表):
2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表): 气体的体积大于________L,小于________L.
气体的体积大于________L,小于________L.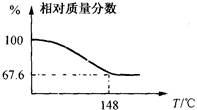
 量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。
量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。 溶于氢氟酸可制得电解法炼铝必需的熔剂冰晶石(Na3AlF6),同时反应中产生一种无色无味的气体,试写出有关化学方程式_________。
溶于氢氟酸可制得电解法炼铝必需的熔剂冰晶石(Na3AlF6),同时反应中产生一种无色无味的气体,试写出有关化学方程式_________。 终产物是 ( )
终产物是 ( )