题目内容
【题目】对于反应N2O4![]() 2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)。下列说法正确的是
2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)。下列说法正确的是
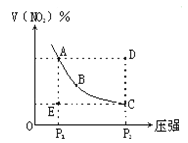
A、A、C两点的正反应速率的关系A>C
B、A、B、C、D、E各状态,V正>V逆的是状态D
C、使E状态从水平方向到达C状态,从理论上来讲,
可选用的条件是从P1突然加压至P2
D、维持P1不变,E→A所需时间为x,维持P2不变,D→C所需
时间为y,则x<y
【答案】C
【解析】
试题分析:A.对于有气体参加的化学反应,压强越大,反应速率越大,由于C点对应的压强大于A点的压强,所以正反应速率A<C,A项错误;B.在图象中,A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等,D点要达到平衡,必须降低NO2的质量分数,也就是使平衡向逆反应方向移动,从而得出v(正)< v(逆),B项错误;C.当快速加压时,平衡未移动,当缓慢加压时,平衡不断地被破坏,但又不断地建立新的平衡,所以“使E状态从水平方向到达C状态”,应突然加压;“由C沿平衡曲线以达A状态”,应缓慢降压,C项正确;D.压强越大反应速率越大,因D点的压强大于E点的,所以D点的反应速率大于E点的反应速率,所需时间x>y,D项错误;答案选C。

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目