题目内容
5.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合,下列关系式中正确的是( )| A. | c (Na+)=2c(CH3COO-)+2c(CH3COOH) | B. | c(H+)=c(CH3COO-)+c(OH-) | ||
| C. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | D. | c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
分析 物质的量浓度相等的CH3COOH 和CH3COONa溶液等体积混合后,结合电荷守恒和物料守恒分析解答.
A、根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c (Na+);
B、电荷守恒分析判断;
C、醋酸电离程度大于醋酸根离子水解程度分析;
D、依据电荷守恒和物料守恒计算分析.
解答 解:A.溶液体积增大一倍,则溶液中醋酸和醋酸钠的浓度降为原来的一半,所以根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c (Na+),故A错误;
B.根据电荷守恒得c(OH-)+c (CH3COO-)=c(H+)+c(Na+),故B错误;
C、醋酸的电离程度大于醋酸根离子的水解程度,离子浓度大小为:c (CH3COO-)>c (Na+)>c(H+)>c(OH-),故C错误;
D、任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(OH-)+c (CH3COO-)=c(H+)+c(Na+),根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c (Na+),带入计算得到c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),故D正确;
故选D.
点评 本题考查了电解质溶液中离子浓度大小分析判断,电荷守恒、物料守恒的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
15.下列变化涉及的反应类型中,属于加成反应的是( )
| A. | 苯→环已烷 | B. | 乙烯→聚乙烯 | C. | 苯→溴苯 | D. | 甲烷→四氯甲烷 |
20.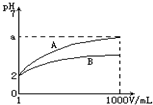 pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
 pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )| A. | A、B溶液浓度一定相等 | B. | 稀释后A溶液酸性比B溶液强 | ||
| C. | a=5时,A是强酸,B是弱酸 | D. | 若A、B都是弱酸,则2<a=5 |
10.下列关于有机物类别说法正确的是( )
| A. | 含有碳碳双键的有机物都属于烯烃 | |
| B. | 一氯甲烷、二氯甲烷、三氯甲烷与四氯甲烷互为同系物 | |
| C. | 两种烃的含碳量相同,则一定互为同分异构体 | |
| D. | 苯酚与苯甲醇都属于烃的含氧衍生物 |
17.下列各组中两个反应的类型相同的是( )
| A. | 苯转化为溴苯、苯酚转化为环己醇 | |
| B. | 由乙醇制溴乙烷、由乙烯制溴乙烷 | |
| C. | 乙烯使溴水褪色、乙醇使酸性重铬酸钾溶液变为蓝绿色 | |
| D. | 由乙炔制氯乙烯、由氯乙烯制聚氯乙烯 |
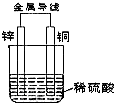 根据如图铜锌原电池示意图,回答下列问题:
根据如图铜锌原电池示意图,回答下列问题: