题目内容
【题目】某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.
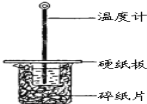
(1)下列说法不正确的是( )
A.该实验也可在保温杯中进行
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是保温、隔热,减少热量损失
D.若将盐酸体积改为60mL,两次实验所求得中和热不相等
(2)若通过实验测定中和热的△H的绝对值常常小于57.3kJ/mol,其原因可能是_________
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
C.量取NaOH溶液的体积时仰视读数
D.用温度计测定盐酸初始温度后,直接测定氢氧化钠溶液的温度
(3)将一定量的稀氨水、稀氢氧化钠溶液、稀氢氧化钡溶液分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为__________;

(4)若将V1mL1.0molL-1 HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由图2可知,氢氧化钠的浓度为 __________ ;
【答案】(1)D (2)ABD (3)ΔH1>ΔH2=ΔH3 (4)1.5mol/L
【解析】
试题分析:(1)A.该实验也可在保温杯中进行,A正确;B.图中实验装置缺少环形玻璃搅拌棒,B正确;C.烧杯间填满碎纸条的作用是保温、隔热,减少热量损失,C正确;D.若将盐酸体积改为60mL,两次实验所求得中和热相等,D错误,答案选D。
(2)A.实验装置保温、隔热效果差,导致热量损失,测量值减小,A正确;B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中导致热量损失,测量值减小,B正确;C.量取NaOH溶液的体积时仰视读数,实际量取的体积增加,测量值偏大,C错误;D.用温度计测定盐酸初始温度后,直接测定氢氧化钠溶液的温度,导致氢氧化钠减少,放出的热量减少,测量值减小,D正确。答案选ABD。
(3)弱电解质中才电离平衡,电离吸热,所以实际放出的热量减少,放热越少,△H越大,则ΔH1、ΔH2、ΔH3的大小关系为ΔH1>ΔH2=ΔH3;
(4)温度最高时说明二者恰好完全反应,所以氢氧化钠的浓度为![]() =1.5mol。
=1.5mol。

 中考解读考点精练系列答案
中考解读考点精练系列答案
