题目内容
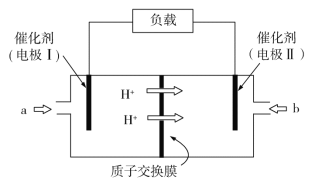
【题目】某新型水系钠离子电池工作原理如图所示。TiO2光电极能使电池在太阳光照下充电,充电时Na2S4 还原为 Na2S。下列说法不正确的是

A. 充电时,太阳能转化为电能,电能又转化为化学能
B. M 是阴离子交换膜
C. 放电时,a 极为负极
D. 充电时,阳极的电极反应式为 3I--2e-=I3-
【答案】B
【解析】
根据题意:TiO2光电极能使电池在太阳光照下充电,所以充电时,太阳能转化为电能,电能又转化为化学能,充电时Na2S4还原为Na2S,放电和充电互为逆过程,所以a是负极,b是电池的正极,在充电时,阳极上发生失电子的氧化反应:3I--2e-=I3-,据此回答。
A.根据题意:TiO2光电极能使电池在太阳光照下充电,所以充电时,太阳能转化为电能,电能又转化为化学能,A正确;
B.根据原电池原理可知,为防止氧化剂和还原剂直接反应,用离子交换膜将两者隔离,而钠离子不参与电池反应,故离子交换膜可允许钠离子自由通过,所以M应该是阳离子交换膜,B错误;C.充电时Na2S4还原为Na2S,放电和充电互为逆过程,所以放电时a是负极,C正确;
D.在充电时,阳极b上发生失电子的氧化反应,根据图示知道电极反应为3I--2e-=I3-,D正确;
故合理选项是B。

练习册系列答案
相关题目