题目内容
【题目】现有下列4种物质:①NO2②Al(OH)3③FeCl2④SiO2
(1)与水反应产生无色气体的是___(填序号,下同),反应的化学方程式为___。
(2)光导纤维的主要成分是___。
(3)既能与酸反应又能与强碱溶液反应的两性氢氧化物是___,该物质与强碱反应的离子方程式为___。
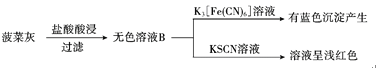
(4)有人预测①与③的溶液能发生化学反应,可能出现的现象是___。
【答案】① 3NO2+H2O=2HNO3+NO ④ ② Al(OH)3+OH-=AlO![]() +2H2O 溶液由浅绿色变为棕黄色;红棕色气体变无色;反应后气体与空气接触变红棕色
+2H2O 溶液由浅绿色变为棕黄色;红棕色气体变无色;反应后气体与空气接触变红棕色
【解析】
(1)NO2与水反应生成HNO3和NO,与水反应产生无色气体的是①,反应的化学方程式为3NO2+H2O=2HNO3+NO。故答案为:①;3NO2+H2O=2HNO3+NO;
(2)光导纤维的主要成分是SiO2。故答案为:④;
(3)既能与酸反应又能与强碱溶液反应的两性氢氧化物是Al(OH)3,Al(OH)3与强碱反应生成偏铝酸根和水,离子方程式为Al(OH)3+OH-=AlO![]() +2H2O。故答案为:②;Al(OH)3+OH-=AlO
+2H2O。故答案为:②;Al(OH)3+OH-=AlO![]() +2H2O;
+2H2O;
(4)①NO2和③FeCl2的溶液能发生化学反应,二氧化氮能将亚铁离子氧化成铁离子、自身被还原成NO,NO在空气中又被氧化成NO2,可能出现的现象是溶液由浅绿色变为棕黄色;红棕色气体变无色;反应后气体与空气接触变红棕色。故答案为:溶液由浅绿色变为棕黄色;红棕色气体变无色;反应后气体与空气接触变红棕色。

 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】温度为T1时,向容积为2 L 的密闭容器甲、乙中分别充入一定量的CO(g)和H2O(g),发生反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
容器 | 甲 | 乙 | ||
反应物 | CO | H2O | CO | H2O |
起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
A. 甲容器中,平衡时,反应放出的热量为16.4 kJ
B. T1时,反应的平衡常数K甲 = 1
C. 平衡时,乙中CO的浓度是甲中的2倍
D. 乙容器中,平衡时CO的转化率约为75%