题目内容
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表
2NO2(g)体系中,n(NO)随时间的变化如表
![]()
(1)下图中表示NO2的变化的曲线是___________。用O2表示从0~2s内该反应的平均速率v=________________________。
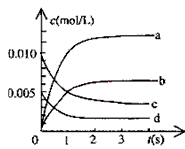
(2)能说明该反应已达到平衡状态的是___________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是_____________ 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
【答案】(1)b;1.5×10-3 mol/(Ls) (2)b、c (3)c
【解析】
试题分析:(1)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO)=(0.020mol-0.007mol)/2L=0.0065mol/L,所以图中表示NO2变化的曲线是b,
故答案为:b;2s内用NO表示的平均反应速率v(NO) = 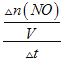 =
= 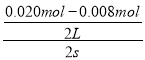 = 3.0 × 10-3molL-1s-1,速率之比等于化学计量数之比,所以v(O2) = 1/2v(NO) = 1/2 × 3.0 × 10-3 molL-1s-1 = 1.5 × 10-3molL-1s-1,故答案为:1.5×10-3molL-1s-1;
= 3.0 × 10-3molL-1s-1,速率之比等于化学计量数之比,所以v(O2) = 1/2v(NO) = 1/2 × 3.0 × 10-3 molL-1s-1 = 1.5 × 10-3molL-1s-1,故答案为:1.5×10-3molL-1s-1;
(2)a、表示同一方向反应速率,v(NO2)自始至终为v(O2)的2倍,不能说明达到平衡,故a错误;b、随反应进行,反应混合气体总的物质的量在减小,气体总物质的量保持不变,说明反应到达平衡,故b正确;c、不同物质表示速率,到达平衡时,正逆速率之比等于化学计量数之比,V逆 (NO):正(O2)=2:1,即V逆(NO)=2v正(O2),故c正确;d、混合气体的总质量不变,容器容积为定值,所以密度自始至终不变,不能说明达到平衡,故d错误;故答案为:bc.
(3)a.及时分离除NO2气体,反应速率变小,错误; b.适当升高温度,反应的反应速率增大,平衡向逆反应方向移动,错误;[]c.增大O2的浓度,反应的反应速率增大,平衡向正反应方向移动,正确; d.选择高效催化剂,反应的反应速率增大,平衡不移动,错误;故选 C.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 碱液 | 过滤 |
B | 乙烷(乙烯) | 氢气 | 加热 |
C | 乙醇(水) | 生石灰 | 蒸馏 |
D | 苯(甲苯) | 蒸馏水 | 分液 |
A. A B. B C. C D. D
