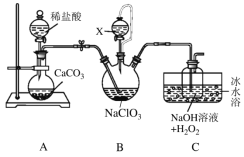
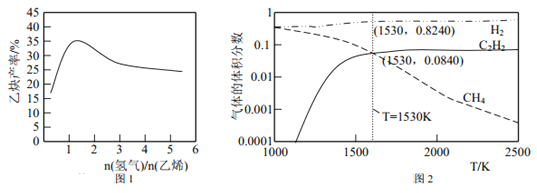
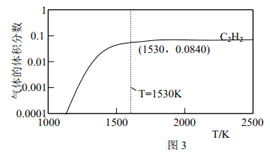
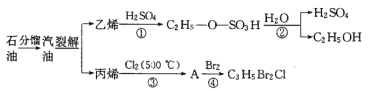
题目内容
【题目】关于热化学方程式CO(g)+![]() O2(g)=CO2(g) H=-283kJmol-1,下列说法正确的是
O2(g)=CO2(g) H=-283kJmol-1,下列说法正确的是
A.一氧化碳和氧气反应放出283 kJ热量
B.1 mol CO和0.5 mol O2反应生成1 mol CO2吸收283 kJ热量
C.2 mol CO(g)和1 mol O2(g)反应生成2 mol CO2(g)时放出566 kJ热量
D.1个CO分子和0.5个O2分子反应吸收283 kJ热量
【答案】C
【解析】
A.反应放出的热量与反应的物质多少有关,未指明反应的物质多少,反应放出的热量不能确定,A错误;
B.根据题意可知1 mol CO和0.5 mol O2反应生成1 mol CO2放出283 kJ热量,B错误;
C.热化学方程式的系数仅表示物质的量,根据题意可知1 mol CO和0.5 mol O2反应生成1 mol CO2放出283 kJ热量,则2 mol CO(g)和1 mol O2(g)反应生成2 mol CO2(g)时放出566 kJ热量,C正确;
D.热化学方程式的系数仅表示物质的量,不能表示分子数目,D错误;
故合理选项是C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目