题目内容
【题目】如图是铜-锌原电池示意图。下列有关该原电池的描述中正确的是( )

A.锌片作正极,不断溶解
B.铜片作负极,有气泡产生
C.负极反应:Zn2++2e-=Zn
D.正极反应:2H++2e-=H2↑
【答案】D
【解析】
Cu、Zn与硫酸构成原电池,电池总反应式为:Zn+H2SO4=ZnSO4+H2↑,Zn为负极、Cu正极,正极发生还原反应,氢气在Cu电极析出。
A.锌电极做负极,不断消耗溶解,故A选项错误。
B.铜电极为正极,发生还原反应,氢气在Cu电极析出,故B选项错误。
C.负极发生的反应是锌做负极失电子发生氧化反应生成锌离子,Zn-2e-=Zn2+,故C选项错误。
D.铜电极为正极,发生还原反应有氢气产生,发生反应2H++2e-=H2↑,故D选项正确。
故答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】双氧水在医疗、军事和工业上用途广泛,工业上合成双氧水的方法有多种,其中一种合成工艺为乙基蒽醌(EAQ)法。
已知:
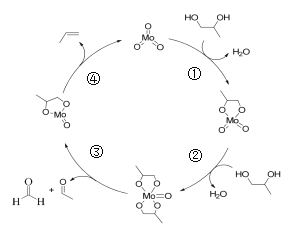
①反应原理为

②工业制备流程如图所示。

③制备过程中,将EAQ溶于有机溶剂中配制成工作液。
请回答下列问题:
(1)该流程中,循环使用的原料为___。
(2)现有甲、乙、丙三种有机溶剂,相关物质的溶解情况如表所示,则配制工作液时,应选用有机溶剂__(填“甲”“乙”或“丙”),原因为___。
物质 | 甲 | 乙 | 丙 |
EAQ | 互溶 | 不溶 | 互溶 |
EHAQ | 互溶 | 不溶 | 互溶 |
H2O2 | 不溶 | 不溶 | 互溶 |
H2O | 不溶 | 不溶 | 互溶 |
(3)“氧化”时,控制温度为45~55℃,原因为___。
(4)“萃取”时,所选用的萃取剂是一种常见的溶剂,其化学名称为__,选用该溶剂作为萃取剂的原因为__。
(5)“净化”的目的是将萃取液中的过氧化氢分离出来,则应选用的分离方法为___。
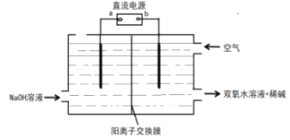
(6)采用电解法制备双氧水的装置示意图如图所示,通入空气的电极的电极反应式___。