题目内容
18.在一定温度下可逆反应2NO2(g)═2NO(g)+O2(g)在体积固定的密闭容器中反应,下列叙述能够说明该反应已经达到平衡状态的是( )| A. | 单位时间内生成amol O2的同时生成2amol NO的状态 | |
| B. | NO2、NO、O2三者物质的量之比为2:2:1的状态 | |
| C. | 混合气体的密度不随时间变化而变化的状态 | |
| D. | 混合气体的平均相对分子质量不随时间变化而变化的状态 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、单位时间内生成amol O2等效于消耗2amol NO同时生成2amol NO的状态,正逆反应速率相等,达平衡状态,故A正确;
B、当体系达平衡状态时,NO2、NO、O2的浓度可能是2:2:1,也可能不是,与各物质的初始浓度及转化率有关,故B错误;
C、密度一直不随时间的变化,故C错误;
D、混合气体的平均相对分子质量不随时间变化而变化的状态,说明气体的总物质的量不变,达平衡状态,故D正确;
故选AD.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
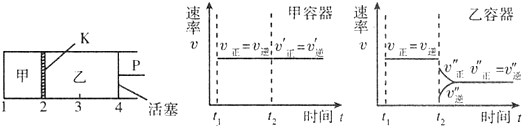
6.一定温度下可逆反应:A(s)+2B(g)F?2C(g)+D(g);△H<O.现将1molA和2mol B加入甲容器中,将4mol C和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )

| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图所示(t1前的反应速率变化已省略) |
13.下列褪色现象中,其中一项与其他三项褪色原理不同的是( )
| A. | 二氧化硫能使酸性高锰酸钾溶液褪色 | |
| B. | 氯水能使甲基橙褪色 | |
| C. | 浓硝酸能使石蕊试液褪色 | |
| D. | 臭氧能使品红溶液褪色 |
3.人工固氮为粮食丰产奠定了基础.下面能实现人工固氮的是( )
| A. | 闪电 | B. | 由氨制硝酸 | C. | 大豆的根瘤 | D. | 合成氨工厂 |
10.下列有关实验现象或亊实解释正确的是 ( )
| 选项 | 实验现象或事实 | 解释 |
| A | 检验待测液中SO42-时,先滴入稀盐酸,再滴入BaCl2溶液 | 先滴入盐酸可排除Ag+、CO32-、SO32-等离子干扰 |
| B | 制备乙酸乙酯时,导管应伸入试管至饱和Na2CO3溶液液面上方 | 乙酸乙酯易溶于碳酸钠溶液,防止发生倒吸 |
| C | 向Fe(NO3)2溶液中加入稀硫酸,试管口有红棕色气体产生 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 含Mg(HCO3)2的硬水长时间充分加热,最终得到的沉淀物的主要成分为Mg(OH)2,而不是MgCO3 | Ksp(MgCO3)<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
7.常温下,下列有说法不正确的是( )
| A. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] | |
| C. | 将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)增大 | |
| D. | 常温下0.1 mol•L-1的下列溶液①NH4Al(SO4)2,②NH4Cl,③NH3•H2O,④CH3COONH4中,c(NH4+)由大到小的顺序是:①>②>④>③ |
8.下列说法正确的是( )
| A. | 在离子化合物中,可能含共价键 | |
| B. | 在共价化合物中,可能含离子键 | |
| C. | 含共价键的化合物一定是共价化合物 | |
| D. | 含离子键的化合物不一定是离子化合物 |