��Ŀ����
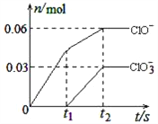
����Ŀ����һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ(��֪��Ӧ���̷���)���������������ֺ���Ԫ�ص����ӣ�����ClO����ClO3���������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ����ͼ��ʾ������˵����ȷ���ǣ� ��
A. ���Լ���Һ��KOH�����ʵ�����0.09mol
B. ClO3�����������������������Ķ��������
C. ������������ClO����ClO3��������Cl2
D. ��Ӧ��ת�Ƶ��ӵ����ʵ�����0.21mol
���𰸡�D
�����������������A������������������Һ��Ӧ���ɴ�����ء��Ȼ��غ�����أ�����ͼ��֪n��ClO-��=0.06mol��n��ClO3-��=0.03mol�����ݵ���ת���غ��֪���ɵ�������n��Cl-��=0.06mol����1-0��+0.03mol����5-0��=0.21mol�����������غ��֪n��K+��=n��Cl-��+n��ClO-��+n��ClO3-��=0.21mol+0.06mol+0.03mol=0.3mol�����������ص����ʵ���=0.3mol��A����B����0��t1��û��ClO3�������ɣ�˵�����¶��йأ�B����C��ClO����ClO3�������ܿ�����Cl2����Ϊ�����ܶ��õ��ӣ�C����D����Ӧ��ת�Ƶ��ӵ����ʵ�����0.21mol��D��ȷ����ѡD

 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�����Ŀ����T��ʱ,������ӦC(s)+H2O(g) ![]() CO(g)+H2(g)��
CO(g)+H2(g)��
��1��T��ʱ,��һ��2L���ܱ������м���4molC��1molH2O(g),5min��Ӧ�ﵽƽ��,C��ת����Ϊ20%��
��0��5min��,��H2O(g)��ʾ��ƽ����Ӧ����Ϊ____________��
�ڸ÷�Ӧ�ﵽƽ��ı�־��______��
a.�����ƽ����Է�����������
b.������ܶȲ���
c.H2O(g)��CO(g)��H2(g)�����ʵ���֮��Ϊ1��1:1
d.����������ʵ�������
��2��T��ʱ,�������ܱ������м�����Ӧ�����ʽ���ʵ��,�м�ĸ���������ɻ�����

���������������ƽ����Է�������һֱ���ֲ��䣬��Ӧ��ʼǰH2O(g)��H2(g)�����ʵ���֮����__________��
�ڷ�Ӧ�ڴﵽƽ��ʱ,�м�ĸ���������λ����________��
a.1��1.5֮�� b.1.5�� c.1.5��2֮��
��3����֪:I.�ƻ�1mol���ۼ�����Ҫ���������±���
���ۼ� | ʯī�е�̼̼�� | H-H | C��O | H-O |
����/kJ | 475.7 | 436 | 1072 | 463 |
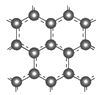
��.ʯī���������η䳲�ṹ��̼ԭ�ӹ��ɣ���ͼ��ʾ:
ijͬѧ����:ͨ������װ��ʵ��C(s)+H2O(g) ![]() CO(g)+H2(g)�ķ�Ӧ��
CO(g)+H2(g)�ķ�Ӧ��
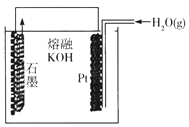
�ٰ��ÿ����Ĺ���,ʯī�缫�����ķ�ӦʽΪ_______________��
��������������?˵������: _______________��