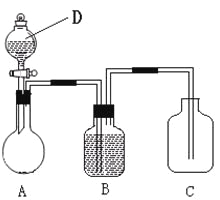
��Ŀ����
����Ŀ��ʵ��������500mL0.2mol��L-1��Na2SO4��Һ���ش��������⣺
��1����д����ʵ����������еĿհ״���
A.����ƽ�ϳ�ȡ___gNa2SO4���壬��������___�У�������������ˮ�ܽ⣻
B.���Ƶõ���ҺС�ĵ�����___ע��___�У�
C.����������ƿ�м�������ˮ��Һ��������ƿ���̶�����1��2cmʱ������___С�ĵμ�����ˮ����Һ��Һ����ʹ���̶���ˮƽ���У�
D.����������ˮϴ���ձ��ڱںͲ�����2��3�Σ�ÿ��ϴ��ҺҲС��ת������ƿ�У�������ҡ�ȣ�
E.�Ǻ�ƿ�����������µߵ���ҡ�ȡ�
��2���ڣ�1�����в����������ȷ˳����(����)___��
��3����������У���ʹ������ҺŨ��ƫ�ߵ���___(����)��
a.�ܽ����ʱ�в���Һ�彦��
b.������ˮʱ�����������˿̶���
C.�ڶ���ʱ�����ӿ̶���
d.����ƿʹ��ǰ�ڱ�մ��ˮ��
���𰸡�14.2 �ձ� ������ 500mL����ƿ ��ͷ�ι� ABDCE c
��������
(1)A������n=CV��m=nM������Ҫ���ʵ��������������ձ����ܽ⣻
B������Һת������ƿʱҪ�ò�����������
C���ý�ͷ�ι�������ƿ�м�Һ��ʱ����ȷ��Һ���̶��ߣ�
(2)��Һ���Ʋ��������У��������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����
(3)������������Һ���ʵ�������Һ�����Ӱ�죬����c=![]() ����������������ҺŨ�ȵ�Ӱ�졣
����������������ҺŨ�ȵ�Ӱ�졣
(1)A��500L 0.2mol/LNa2SO4��Һ�������ʵ����ʵ����ʵ���Ϊ��0.2mol/L��0.5L=0.1mol��������ҪgNa2SO4�����������0.1mol��142g/mol=14.2g�������õ������ƹ�������ձ����ܽ⣻
B������Һת������ƿʱҪ�ò����������������Ƶõ���ҺС�ĵ����Ų�����ע��500mL������ƿ�У�
C���ý�ͷ�ι�������ƿ�м�Һ��ʱ����ȷ��Һ���̶��ߣ���������ƿ�м�������ˮ��Һ��������ƿ���̶�����1��2cmʱ�����ý�ͷ�ι�С�ĵμ�����ˮ����Һ��Һ����ʹ���̶���ˮƽ���У�
(2)��Һ���Ʋ��������У��������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����������������ȷ˳����ABDCE��
(3)a���ܽ����ʱ�в���Һ�彦�����������Ƶ����ʵ�����С����������Ũ��ƫ�ͣ���a��ѡ��
b��������ˮʱ�����������˿̶��ߣ���Һ�����ƫ��ʹ������ҺŨ��ƫ�ͣ���b��ѡ��
c���ڶ���ʱ�����ӿ̶��ߣ���Һ�����ƫС��ʹ������ҺŨ��ƫ�ߣ���cѡ��
d������ƿʹ��ǰ�ڱ�մ��ˮ�飬�����ʺ��ܼ�����Ӱ�죬��������Ũ�Ȳ��䣬��d��ѡ��
�ʴ�Ϊ��c��

����Ŀ��(1)0.3mol����̬����ȼ��������(B2H6)��������ȼ�գ����ɹ�̬�������������Һ̬ˮ���ų�649.5kJ���������Ȼ�ѧ����ʽΪ________��
(2)�����ٷɻ���ƽ�������ʱ��β���е�NO���ƻ������㡣��ѧ�������о����ô�������β���е�NO��COת���CO2��N2����ѧ����ʽΪ��![]() ��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��������崫������ò�ͬʱ���NO��COŨ�������
��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��������崫������ò�ͬʱ���NO��COŨ�������
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/ mol��L-1 | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
c(CO)/mol��L-1 | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
��ش��������⣺
��ǰ2s�ڵ�ƽ����Ӧ������(N2)��____��
�����������£��÷�Ӧ��ƽ�ⳣ��Ϊ____��
�����������£����ijʱ�̷�Ӧ��ϵ�и����ʵ����ʵ���Ũ�Ⱦ�Ϊ0.01mol/L�����ʱ��Ӧ����___״̬��(����ƽ�����������ҽ������������������)
(3)ʵ���ҳ���0.10mol/L KMnO4��������Һ���ⶨH2C2O4��Ʒ�Ĵ���(��Һ�δ���Һ)���䷴Ӧԭ��Ϊ��5H2C2O4+2MnO4-+6H+=10CO2��+2Mn2++8H2O��
��KMnO4��ҺӦװ��____(������ʽ��������ʽ��)�ζ��ܣ�
����ˮϴ���ζ��ܺ�ֱ��װ���Һ����ⶨ�����____��(����ƫ��������ƫС������������)