题目内容
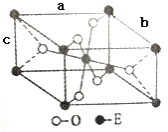
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________。![]()
![]()
![]()
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________。将所得沉淀过滤、洗涤、灼烧,可得到___________g固体。
【答案】过氧化钠 Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落  BC 2Na + 2H2O+ Cu2+ === Cu(OH)2 ↓ + 2Na+ + H2 ↑
BC 2Na + 2H2O+ Cu2+ === Cu(OH)2 ↓ + 2Na+ + H2 ↑ ![]()
【解析】
A的一种单质是自然界硬度最大的物质,是金刚石,则A为碳;B与C的单质在加热条件下反应生成淡黄色化合物X,为过氧化钠,则B为氧,C为钠;D的单质既能与盐酸、也能与NaOH溶液反应生成H2,说明D为铝,E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y,说明E为铁,生成四氧化三铁。
(1)根据分析得到物质X的名称为过氧化钠,故答案为过氧化钠。
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落,故答案为:Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落。
(3) E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:
 ,故答案为:
,故答案为:![]() 。
。
(4)ag 钠投入足量CuSO4溶液中,“浮”、“熔”、“游”、“嘶”“蓝”,因此实验现象正确的是B.熔化成银色光亮的小球,C.小球四处游动发出”嘶嘶”的声音,可能的离子方程式为2Na + 2H2O+ Cu2+ =Cu(OH)2 ↓ + 2Na+ + H2 ↑,
根据守恒2Na ——Cu(OH)2 ↓——CuO
46g 80g
ag xg
46g:ag = 80g:xg
解得x =![]() ,故答案为:BC;2Na + 2H2O+Cu2+=Cu(OH)2 ↓+2Na++H2 ↑;
,故答案为:BC;2Na + 2H2O+Cu2+=Cu(OH)2 ↓+2Na++H2 ↑;![]() 。
。

 阅读快车系列答案
阅读快车系列答案