题目内容
如下图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰。现欲利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答以下问题。
(1)选用A装置可制取的气体有 ;选用B装置可制取的气体有 ;通常选用C装置制取的气体有 。若用亚硫酸钠和浓硫酸来制取二氧化硫气体应选用装置 (填装置的编号字母)。
(2)写出利用上述有关药品制取氯气的化学方程式: 。
(3)若要制得干燥的氨气,可选用下列干燥剂中的 (填序号)。
A.生石灰 B.浓硫酸 C.五氧化二磷
(4)标号①的仪器除可用于在气体发生装置中添加试剂外,在实验中常用于 (填实验操作名称)。
(1)NH3;CO2,H2;Cl2;B (2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O (3)A
MnCl2+Cl2↑+2H2O (3)A
(4)分液
解析试题分析:(1)选用A装置是固体与固体混合加热制取气体的装置。可制取的气体有NH3;固体与液体混合在不加热时制取气体的装置。选用B装置可制取的气体有CO2,H2;通常选用C装置制取的气体应该是固体与液体混合加热制取气体的装置。选用该装置制取的气体有Cl2;若用亚硫酸钠和浓硫酸来制取二氧化硫气体,由于是固体与液体混合不需要加热制取气体,所以应选用装置B。(2)制取氯气的化学方程式:为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O 。(3)若要制得干燥的氨气,由于氨气的水溶液显碱性,所以要用碱性干燥剂来干燥。因此选项为A。(4)标号①的仪器除可用于在气体发生装置中添加试剂外,在实验中常用于分离互不相溶的两层液体混合物,该实验操作为分液。
MnCl2+Cl2↑+2H2O 。(3)若要制得干燥的氨气,由于氨气的水溶液显碱性,所以要用碱性干燥剂来干燥。因此选项为A。(4)标号①的仪器除可用于在气体发生装置中添加试剂外,在实验中常用于分离互不相溶的两层液体混合物,该实验操作为分液。
考点:考查气体制取装置的选择、反应原理、气体的干燥即试剂的添加等实验操作的知识。

用下图装置不能完成气体制取任务的是
| A.过氧化钠和水反应制取氧气 |
| B.生石灰和浓氨水反应制取氨气 |
| C.二氧化锰和浓盐酸反应制取氯气 |
| D.碳化钙和饱和食盐水反应制取乙炔 |
下列反应适用于实验室制备氧气的是
①高锰酸钾热分解 2KMnO4 K2MnO4+MnO2+ O2↑
K2MnO4+MnO2+ O2↑
②硝酸铵热分解 2NH4NO3 4H2O+2N2↑+ O2↑
4H2O+2N2↑+ O2↑
③过氧化氢催化分解 2H2O2 2H2O +O2↑
2H2O +O2↑
④二氧化氮热分解 2NO2 2NO+ O2↑
2NO+ O2↑
| A.只有① | B.①和② | C.①和③ | D.①③④ |
过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
Ⅰ.过氧化钙晶体的制备。
工业上生产CaO2·8H2O的主要流程如下: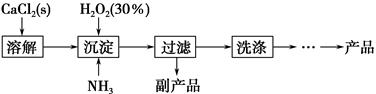
(1)用上述方法制取CaO2·8H2O的化学方程式是_________________________________。
(2)沉淀时常用冰水控制温度在10 ℃以下和通入过量的NH3,其可能原因分别是①__________________________;②_____________________________。
Ⅱ.过氧化钙晶体含量的测定。
准确称取0.300 0 g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.020 0 mol·L-1 KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
滴定终点观察到的现象为_______________________________________。
(4)根据表中数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)。
KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.300 0 | 1.02 | 24.04 |
| 2 | 0.300 0 | 2.00 | 25.03 |
| 3 | 0.300 0 | 0.20 | 23.24 |






 N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂: