题目内容
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号) 。
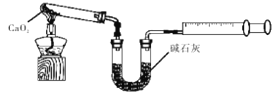
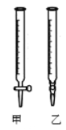
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视 。判断到达滴定终点的现象是:锥形瓶中溶液 。
(5)以下是实验数据记录表
滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
通过计算可得,该盐酸浓度为:______ molL-1(计算结果保留4位小数)
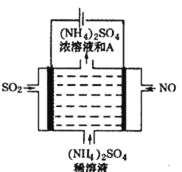
II、利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤1:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤2:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤:1相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
则BaCl2溶液浓度为______________________ mol·L-1。若步骤2中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将___________(填“偏大”或“偏小”)。
【答案】I、(1)①④;(2)乙;(3)B;
(4)锥形瓶内颜色;由无色变成浅红色,且半分钟内不变色。(5)0.1631;
II、(V0b-V1b)/y ;偏大。
【解析】
试题分析:(1)①根据碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上,碱式滴定管未用标准氢氧化钠溶液润洗就直接注入标准NaOH溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=V(标准)×c(标准) ÷V(待测),可知c(标准)偏大;④酸碱指示剂酚酞是弱电解质,也会反应消耗酸或碱,为了减少实验误差,酚酞一般滴加1滴或2滴,错误;其余操作正确;(2)NaOH是碱,容易与玻璃中的SiO2发生反应,所以应该装在碱式滴定管乙中;(3)A.在锥形瓶装液前,留有少量蒸馏水,由于不影响酸、碱的物质的量,所以对滴定操作无影响,错误;B.滴定前,滴定管尖嘴有气泡,滴定后无气泡,使标准溶液体积偏大,导致待测溶液的浓度偏高,正确;C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗,操作正确,不会产生误差,错误;D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失,则待测溶液体积偏少,反应消耗标准酸溶液的体积偏小,使测得浓度偏低,错误。(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内颜色;判断到达滴定终点的现象是:锥形瓶中溶液由无色变成浅红色,且半分钟内不变色。(5)酸碱发生中和反应时二者的物质的量相等。根据实验数据可知,第一次实验数据误差太大,舍弃,V(NaOH)= (16.30+16.32)÷2=16.31mL,c(NaOH)·V(NaOH)=c(HCl)·V(HCl),所以c(HCl)=[ c(NaOH)·V(NaOH)]÷V(HCl)= [0.2000 mol·L-1×16.31mL]÷20.00mL=0.1631mol/L;II、根据方程式可知氢离子的物质的量与溶液中Ba2+的物质的量相等。步骤Ⅱ:待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL,则发生2CrO42-+2H+=Cr2O72-+H2O的盐酸的物质的量为:V1×10-3×bmol,步骤Ⅰ:用b molL-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL,加入的总盐酸的物质的量:V0×10-3×bmol,Ba2++CrO42-=BaCrO4↓,与Ba2+反应的CrO42-的物质的量为V0×10-3×bmol-V1×10-3×bmol=(V0 -V1)b×10-3mol,步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,所以BaCl2溶液的浓度为:(V0 -V1)b×10-3mol ÷y×103mol/L=(V0b-V1b)/ymol/L;若步骤Ⅱ中滴加盐酸时有少量待测液溅出,V1减小,则Ba2+浓度测量值将偏大。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案