题目内容
【题目】下表是元素周期表的一部分。

已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
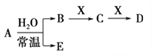
(1)元素⑧的最高价氧化物对应水化物的化学式是_________________________。
(2)元素⑤与As两种元素中,简单气态氢化物较稳定的是___________(填化学式)。
(3)元素②⑥⑦的简单离子半径由大到小的顺序是___________(用化学符号表示)。
(4)元素③的单质与元素②的最高价氧化物对应的水化物反应的离子方程式是________________。
(5)若A为红棕色气体,则X、D的化学式分别为___________、___________。
【答案】 Ca(OH)2 NH3 Cl- >O2- >Na+ 2A1+2OH-+2H2O=2AlO2- +3H2↑ Fe Fe(NO 3)2
【解析】根据元素周期表,可确定①为H、②为Na、③为Al、④为C、⑤为N、⑥为O、⑦为Cl、⑧为Ca;
(1)根据元素周期表可确定⑧是钙,元素⑧的最高价氧化物对应水化物的化学式是 Ca(OH)2 ;(2)⑤是N,与As在同一主族,简单气态氢化物较稳定的是NH3,(3)元素②⑥⑦的简单离子半径由大到小的顺序是Cl- >O2- >Na+ ;(4)元素③的单质Al与元素②的最高价氧化物对应的水化物NaOH反应的离子方程式是2A1+2OH-+2H2O=2AlO2- +3H2↑ ;(5)A红棕色气体,在常温下与水反应生成氧化物,可确定A是NO2,B是HNO3,C是Fe(NO3)3 ,E是NO,则X是Fe,D为Fe(NO3)2 。

练习册系列答案
相关题目