题目内容
14.0.5L 1mol/L FeCl3溶液与3L 0.5mol/L KCl溶液中的Cl-的数目之比( )| A. | 1:6 | B. | 1:1 | C. | 2:1 | D. | 3:1 |
分析 1mol/L FeCl3溶液中Cl-的浓度为3mol/L,0.5mol/L KCl溶液中的Cl-浓度为0.5mol/L,根据n=cV计算判断.
解答 解:0.5L 1mol/L FeCl3溶液中Cl-的物质的量为0.5L×1mol/L×3=1.5mol,
3L 0.5mol/L KCl溶液中的Cl-的物质的量为3L×0.5mol/L=1.5mol,
故二者含有Cl-的数目之比为1.5mol:1.5mol=1:1,
故选B.
点评 本题考查物质的量浓度有关计算,比较基础,关键是明确氯离子浓度与电解质浓度关系.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
4.关于如图所示装置的叙述,正确的是( )
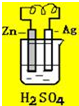

| A. | 银是负极,银片上有气泡产生 | B. | 锌片质量逐渐减少,银片质量不变 | ||
| C. | 电流从锌片经导线流向银片 | D. | 氢离子在锌片上被还原 |
5.下列表示物质结构的化学用语或模型正确的是( )
| A. | 羟基的电子式: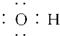 | B. | 溴乙烷的电子式: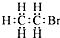 | ||
| C. | 乙醇的结构简式:CH3CH2OH | D. | CH4分子的球棍模型: |
2.下列方法可使海水转化为饮用水的是( )
| A. | 过滤 | B. | 蒸馏 | C. | 活性炭吸附 | D. | 静置沉淀 |
9.我国加碘食盐中加的碘是( )
| A. | KI | B. | KIO3 | C. | I2 | D. | NaI |
6.下列措施可以提高燃料燃烧效果的是( )
①固体燃料粉碎 ②液体燃料雾化 ③煤经气化处理 ④通入足量的空气⑤提高燃料的着火点 ⑥降低燃料的着火点.
①固体燃料粉碎 ②液体燃料雾化 ③煤经气化处理 ④通入足量的空气⑤提高燃料的着火点 ⑥降低燃料的着火点.
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ③④⑤⑥ | D. | ①②③④ |