��Ŀ����
����Ŀ��I����ˮ��������Ȼ���������ص��ƻ����ã�������ˮ��Ⱦ�����̲��ݻ���
(1)ij�����������ķ�ˮ�к���Fe2+��Mn2+�Ƚ������ӣ����ù������[(NH4)2S2O8]������ȥ��
�ٹ��������Mn2+��Ӧ����MnO2�����ӷ���ʽΪ__________��
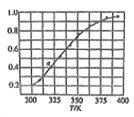
���¶���Fe2+��Mn2+�����̶�֮��Ĺ�ϵ��ͼ��ʾ:

ʵ�������Ӧ���¶ȿ�����_________��
Fe2+��Mn2+���������γɽ�����״���ӣ����������̿�������������̿��Ŀ��Ϊ_______��
(2)����ij����ɸ��������NH3���ѳ�������NO��NO2,�䷴Ӧ������ͼ��ʾ��A�������ʵĻ�ѧʽΪN2��__________��

(3)��ҵ�Ϸ�����SO2����Na2CO3��Һ���գ���Ӧ��������Һ��ɱ仯��ͼ��ʾ��

�����ճ���(ͼ��A����ǰ)��Ӧ�Ļ�ѧ����ʽΪ__________��
��C�����B���ԭ����__________��
���о����֣�NOx��SO2����������Ҫ�ɷ֡�
��֪��N2(g)+O2(g)=2NO(g) ��H=+1805kJ/mol��
C(s)+O2(g)=CO2(g) ��H=-393.5kJ/mol��
2C(s)+O2(g)=2CO(g) ��H-221.0kJ/mol��
(4)ij��Ӧ��ƽ�ⳣ������ʽ![]() ,��д���˷�Ӧ���Ȼ�ѧ����ʽ:__________��
,��д���˷�Ӧ���Ȼ�ѧ����ʽ:__________��
(5)����Ⱥ����ܱ������г��������NO��CO���з�Ӧ�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����_______(�����)��
a.�����е�ѹǿ���� b.2v��(CO)=v��(N2)
c.�����ƽ����Է�����������34.2���� d.�÷�Ӧƽ�ⳣ�����ֲ���
e.NO��CO������ȱ��ֲ���
(6)2SO(g)![]() 2SO2(g)+O2(g),��һ������SO3��������ܱ������У������ƽ��ת�������¶ȱ仯��ͼ��ʾ��ͼ��a���Ӧ�¶��£���֪SO3����ʼѹǿΪP0,���¶��·�Ӧ��ƽ�ⳣ��Kp=____(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
2SO2(g)+O2(g),��һ������SO3��������ܱ������У������ƽ��ת�������¶ȱ仯��ͼ��ʾ��ͼ��a���Ӧ�¶��£���֪SO3����ʼѹǿΪP0,���¶��·�Ӧ��ƽ�ⳣ��Kp=____(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
���𰸡� S2O82-+2H2O+Mn2+=4H++2SO42-+MnO2�� 80��(80��-85���������) �������������γɳ��� H2O 2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3 ������Ԫ���غ㣬NaHSO3�����ʵ�����Na2CO3��2��������NaHSO3�����������������ʹ� 2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��H=-746.5KJ/mol acd 4P0/54
N2(g)+2CO2(g)��H=-746.5KJ/mol acd 4P0/54
��������I��(1)�ٹ��������Mn2+��Ӧ����MnO2,����������ӱ�����Ϊ�����,��Ӧ�����ӷ���ʽΪ��S2O82-+2H2O+Mn2+=4H++2SO42-+MnO2������ͼ���������֪��80�����ҡ�Fe2+��Mn2+�����̶��Ѿ��ܴ�,���±仯����,ʵ�������Ӧ���¶ȿ�����80��(80��-85���������), Fe2+��Mn2+���������γɽ�����״����,���������̿����,�������̿��Ŀ��Ϊ�������������γɳ�����(2)ͼʾ��Ӧ��������A�ķ�ӦΪ![]() ,ԭ���غ��ж�AΪN2��H2O��(3)����ͼ����֪��,���ڷ�Ӧ(ͼ��A����ǰ)̼�������������Ӧ����̼����������������,��Ӧ�Ļ�ѧ����ʽΪ: 2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3 ,�ڸ�����Ԫ���غ㣬NaHSO3�����ʵ�����Na2CO3��2��������NaHSO3�����������������ʹ� �� �� (4) ƽ�ⳣ������ʽΪ������Ũ�ȵ���֮���뷴Ӧ��Ũ�ȵ���֮���ı�ֵ������
,ԭ���غ��ж�AΪN2��H2O��(3)����ͼ����֪��,���ڷ�Ӧ(ͼ��A����ǰ)̼�������������Ӧ����̼����������������,��Ӧ�Ļ�ѧ����ʽΪ: 2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3 ,�ڸ�����Ԫ���غ㣬NaHSO3�����ʵ�����Na2CO3��2��������NaHSO3�����������������ʹ� �� �� (4) ƽ�ⳣ������ʽΪ������Ũ�ȵ���֮���뷴Ӧ��Ũ�ȵ���֮���ı�ֵ������![]() ����֪�˷�Ӧ���Ȼ�ѧ����ʽΪ2NO(g)+2CO(g)
����֪�˷�Ӧ���Ȼ�ѧ����ʽΪ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��Ȼ���ٸ��ݸ�˹���ɣ���Ӧ��-�ڡ�2-�٣��ɵá�H=�C746.5KJ/mol�����Ը÷�Ӧ���Ȼ�ѧ����ʽΪ2NO(g)+2CO(g)
N2(g)+2CO2(g)��Ȼ���ٸ��ݸ�˹���ɣ���Ӧ��-�ڡ�2-�٣��ɵá�H=�C746.5KJ/mol�����Ը÷�Ӧ���Ȼ�ѧ����ʽΪ2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ��H=�C746.5KJ/mol��5���÷�ӦΪ��Ӧǰ����������ʵ����б仯�ķ�Ӧ���������е�ѹǿ����ʱ��������ʵ������䣬˵����Ӧ�ﵽ��ѧƽ��״̬��a��ȷ�����ʺ�ϵ�������ȣ�ӦΪv����CO��= 2v����N2����b����Ӧǰ����������������䣬����������ڷ����仯����������������ٷ����仯�������ƽ����Է�������Ϊ��ֵ����Ӧ����ѧƽ��״̬��c��ȷ���÷�ӦΪ���ȷ�Ӧ�����¶Ȳ��ٷ����ı䣬ƽ�ⳣ�����ֲ��䣬�ﵽƽ��״̬��d��ȷ��NO��CO���ַ�Ӧ�ǰ���1:1Ͷ�ϡ�1:1��Ӧ���κ�ʱ��ʣ���������1:1�����ж���Ӧ�Ƿ�ﵽ��ѧƽ��״̬��e������ȷѡ��acd����6������ʼSO3Ϊamol,���������Ϣ��
N2(g)+2CO2(g) ��H=�C746.5KJ/mol��5���÷�ӦΪ��Ӧǰ����������ʵ����б仯�ķ�Ӧ���������е�ѹǿ����ʱ��������ʵ������䣬˵����Ӧ�ﵽ��ѧƽ��״̬��a��ȷ�����ʺ�ϵ�������ȣ�ӦΪv����CO��= 2v����N2����b����Ӧǰ����������������䣬����������ڷ����仯����������������ٷ����仯�������ƽ����Է�������Ϊ��ֵ����Ӧ����ѧƽ��״̬��c��ȷ���÷�ӦΪ���ȷ�Ӧ�����¶Ȳ��ٷ����ı䣬ƽ�ⳣ�����ֲ��䣬�ﵽƽ��״̬��d��ȷ��NO��CO���ַ�Ӧ�ǰ���1:1Ͷ�ϡ�1:1��Ӧ���κ�ʱ��ʣ���������1:1�����ж���Ӧ�Ƿ�ﵽ��ѧƽ��״̬��e������ȷѡ��acd����6������ʼSO3Ϊamol,���������Ϣ��
2SO3(g)![]() 2SO2(g)+O2(g)��
2SO2(g)+O2(g)��
��ʼ��a 00
�仯�� 0.4a0.4a0.2 a
ƽ���� 0.6a0.4 a 0.2 a
��Ӧ�ﵽƽ��������ѹǿΪa/(0.6a+0.4 a+ 0.2 a)=P0/p��ƽ�⣩��p��ƽ�⣩=1.2P0��SO3���ʵ���������0.6a/(0.6a+0.4 a+ 0.2 a)=1/2;��SO2���ʵ���������0.4 a /(0.6a+0.4 a+ 0.2 a)=1/3��O2���ʵ�������: 0.2 a/(0.6a+0.4 a+ 0.2 a)=1/6�����¶��·�Ӧ��ƽ�ⳣ��KP=��1/6��p��ƽ�⣩������1/3��p��ƽ�⣩��2/(1/2��p��ƽ�⣩��2=4P0/45

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�