题目内容
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:
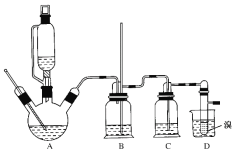
有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是________。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____________。
(3)在装置C中应加入NaOH溶液,其目的是_________。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是_______。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用______洗涤除去;若产物中有少量副产物乙醚,可用_____(填操作方法名称)的方法除去。
(6)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___________。
【答案】防暴沸 减少副产物乙醚生成 B中水面会下降,玻璃管中的水柱会上升,甚至溢出 除去乙烯中带出的酸性气体(或答除去CO2、SO2) D中试管的溴全部褪色 下 氢氧化钠溶液 蒸馏 66.7%
【解析】
装置A中乙醇和浓硫酸加热到170℃生成乙烯气体,装置B平衡气压,防止倒吸以外,还可判断装置是否堵塞;装置C中放入氢氧化钠溶液除去乙醇、浓硫酸反应可能生成的酸性气体二氧化碳、二氧化硫,装置D中乙烯和溴反应生成1,2-二溴乙烷。
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,加入碎瓷片可以防暴沸。乙醇在浓硫酸存在下加热到140℃脱水生成乙醚2CH3CH2OH![]() CH3CH2OCH2CH3+H2O, 170℃生成乙烯,为减少副产物乙醚生成,要尽可能迅速地把反应温度提高到170℃左右;
CH3CH2OCH2CH3+H2O, 170℃生成乙烯,为减少副产物乙醚生成,要尽可能迅速地把反应温度提高到170℃左右;
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中压强增大,B中水面会下降,玻璃管中的水柱会上升,甚至溢出;
(3) 浓硫酸具有脱水性、强氧化性,乙醇、浓硫酸可能生成的酸性气体二氧化碳、二氧化硫,在装置C中加入NaOH溶液,其目的是除去乙烯中带出的酸性气体;
(4)装置D中小试管内盛有液溴,若D中试管的溴全部褪色,可知反应已经结束;
(5) 1,2—二溴乙烷难溶于水、密度大于水,将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下;Br2和氢氧化钠反应生成可溶于水的溴化钠、次溴酸钠,若产物中有少量未反应的Br2,最好用氢氧化钠溶液洗涤除去;1,2—二溴乙烷、乙醚的沸点不同,若产物中有少量副产物乙醚,可用蒸馏的方法除去。
(6) 12.0g溴的物质的量是0.075mol,理论生成0.075mol 1,2—二溴乙烷,若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为![]() 66.7%。
66.7%。

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案