题目内容
【题目】在下列给定条件的溶液中, 一定能大量共存的离子组是
A.无色溶液中:K+、Cu2+ 、NO![]() 、Cl-
、Cl-
B.常温下,![]() =0.1的溶液中:Na+、K+、AlO2-、CO
=0.1的溶液中:Na+、K+、AlO2-、CO![]()
C.0. l molL-1的FeCl2溶液中 :K+、SO![]() 、Mg2+、MnO
、Mg2+、MnO![]()
D.Na2S溶液中:SO![]() 、H+、Cl-、Cu2+
、H+、Cl-、Cu2+
【答案】B
【解析】
A.Cu2+为蓝色,不能在无色溶液中大量共存,A不符合题意;
B.常温下,![]() =0.1的溶液呈碱性,溶液中含有OH-,Na+、K+、AlO2-、CO
=0.1的溶液呈碱性,溶液中含有OH-,Na+、K+、AlO2-、CO![]() 均不与OH-反应且相互不反应,能够大量共存,B符合题意;
均不与OH-反应且相互不反应,能够大量共存,B符合题意;
C.Fe2+会被MnO![]() 氧化而不能共存,C不符合题意;
氧化而不能共存,C不符合题意;
D.Cu2+与Na2S会生成CuS沉淀而不能共存,D不符合题意;
答案选B。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
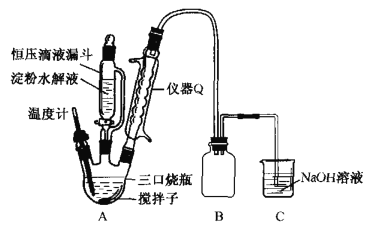
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:
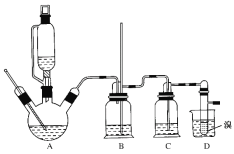
有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是________。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____________。
(3)在装置C中应加入NaOH溶液,其目的是_________。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是_______。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用______洗涤除去;若产物中有少量副产物乙醚,可用_____(填操作方法名称)的方法除去。
(6)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___________。
【题目】下列实验的操作、现象和结论均正确的是
实验操作 | 实验现象 | 实验结论, | |
A | 向FeCl3和 KSCN的混合溶液中滴加NaOH溶液 | 混合溶液颜色逐渐变浅,有红褐色沉淀产生 | Fe3+与SCN-生成Fe(SCN)3是可逆反应 |
B | 将密封有红棕色NO2气体的圆底烧瓶浸入冰水中 | 气体颜色变浅 | 反应2NO2 |
C | 分别向0.1 mol·L- 1的醋酸和饱和硼酸溶液中滴加等浓度的Na2CO3溶液 | 醋酸溶液中有气泡产生,硼酸溶液中无气泡 | 酸性:硼酸>醋酸>碳酸 |
D | 将0.1 mol·L-1AgNO3溶液和0.05mol·L-1NaCl溶液等体积混合,再向混合液中滴入0.05 mol·L-1NaI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
A.AB.BC.CD.D
【题目】锰钢是工业上非常重要的一 种合金, 其主要成分锰是用软锰矿(主要成分为MnO2,还含有少量Al2O3、MgO、SiO2)为原料制备的,某种生产工艺流程如下图所示 :
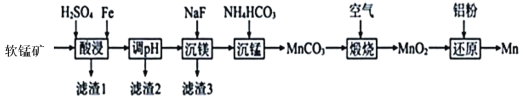
已知:MnO2不溶于稀硫酸,但它可以在酸性条件下和一些还原剂反应生成 Mn2+。
难溶物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 |
溶度积常数 | 4.0×10-38 | 1.0×10-33 | 1.8×10-11 | 1.8×10-13 |
(1)为了提高锰的浸出率 ,通常需要将软锰矿_______; 酸浸时 MnO2 溶解的离子反应方程式是____________________。
(2)滤渣 2 的主要成分是____________(填化学式)。
(3)沉锰时发生的主要离子反应方程式是________; 沉锰后需要对所得的沉淀进行过滤、洗涤操作,如何检验沉淀己洗净?________________。