��Ŀ����
����Ŀ��2019��ŵ������ѧ����������ӵ������LiFePO4(���������) ������ӵ�ص�һ�ֵ缫���ϣ���ͨ�����з����Ʊ���
����һ��2FePO4(s)+Li2 CO3(s)+2C(s)2LiFePO4(s)+3CO(g)
(1)�÷�Ӧ��ƽ�ⳣ������ʽΪ_____�������ݻ�����������У�������Ӧ�ﵽƽ��ʱ��һ����̼��Ũ��ΪamolL��1���ٳ���bmolһ����̼����ƽ����_____�����ƶ����ﵽ��ƽ��ʱ��һ����̼��Ũ��Ϊ_____��
(2)һ���¶��£���2L�ܱ������з���������Ӧ����Ӧ���е�20minʱ�������ڹ��������������5.6g����0��20min��һ����̼��ƽ����Ӧ������_____��
��������LiFePO4����ͨ��(NH4)2Fe(SO4)2��H3PO4��Li OH��Һ������������Ӧ�����ó�����80����ո�����³��Ͷ��Ƶá�
(3)�������Ƽ��Ա�������﮼���ǿ������Ԫ��������֪ʶ˵������_____��
(4)��������ӦͶ��ʱ������(NH4)2Fe(SO4)2��LiOH��Һֱ�ӻ�ϣ���ԭ����_____��
(5)��������﮵���ܷ�ӦΪ��FePO4+Li![]() LiFePO4���ŵ�ʱ������Ϊ_____(��д��ѧʽ)�����øõ�ص�ⱥ��ʳ��ˮ(���ص缫��Ϊ���Ե缫)����������������4480mL����(��״��)����ʱ���õ������﮵�����Ϊ_____��
LiFePO4���ŵ�ʱ������Ϊ_____(��д��ѧʽ)�����øõ�ص�ⱥ��ʳ��ˮ(���ص缫��Ϊ���Ե缫)����������������4480mL����(��״��)����ʱ���õ������﮵�����Ϊ_____��
���𰸡�K��c3(CO) �� amolL��1 0.005mol/(Lmin) ͬһ���壬���ϵ��£�Ԫ������������Ӧ��ˮ�����������ǿ ��ֹ�γɸ��ױ�����������������(�����������ڼ��������¸��ױ�����) Li 1.4g
��������
(1)����ʽ��ֻ��COΪ���壬ƽ�ⳣ��ΪCOŨ�ȵ����η���COŨ������ƽ�������ƶ�����Ϊƽ�ⳣ���������¶ȵĺ������¶Ȳ��䣬ƽ�ⳣ�����䣬�ʴﵽƽ��ʱ��COŨ�Ȳ��䣻
(2)��Ӧ���е�20minʱ�������ڹ��������������5.6g��˵������5.6gCO���ɼ���CO�����ʵ���Ũ�ȣ��������㷴Ӧ���ʣ�
(3)Ԫ�صĽ�����Խǿ����Ӧ������������ˮ����ļ���Խǿ��
(4)(NH4)2Fe(SO4)2��LiOH��Һֱ�ӻ�ϣ��������������������������������ȶ���
(5)��طŵ�ʱԭ���ԭ����Liʧ���ӷ���������Ӧ��ԭ��ظ�����FePO4�������õ����ӷ�����ԭ��Ӧ����LiFePO4����ϸ��ݵ�ⱥ��ʳ��ˮ����ʽ���м������ת�ƣ����ݵ����غ�͵缫��Ӧ��������﮵�������
(1)����ʽ��ֻ��COΪ���壬��K��c3(CO)��COŨ������ƽ�������ƶ����������¶Ȳ��䣬��ƽ�ⳣ�����䣬�ʴﵽƽ��ʱ��COŨ�Ȳ��䣬��ΪamolL��1���ʴ�Ϊ��K��c3(CO)���棻amolL��1��
(2)��Ӧ���е�20minʱ�������ڹ��������������5.6g��˵��������5.6gCO����c(CO)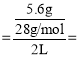 0.1mol/L��
0.1mol/L��![]() 0.005mol/(Lmin)���ʴ�Ϊ��0.005mol/(Lmin)��
0.005mol/(Lmin)���ʴ�Ϊ��0.005mol/(Lmin)��
(3)Li�����ڱ���λ��ͬһ�����Ԫ��Na���Ϸ��������ϵ��£�Ԫ�صĽ�������ǿ��Ԫ�صĽ�����Խǿ����Ӧ������������ˮ����ļ��Ծ�Խǿ�����������Ƽ��Ա�������﮼���ǿ���ʴ�Ϊ��ͬһ���壬���ϵ��£�Ԫ������������Ӧ��ˮ�����������ǿ��
(4)(NH4)2Fe(SO4)2��LiOH��Һֱ�ӻ�ϣ��������������������������������ȶ����ױ����������������������ʴ�Ϊ����ֹ�γɸ��ױ�����������������(�����������ڼ��������¸��ױ�����)��
(5)��طŵ�ʱ��Liʧ���ӷ���������Ӧ������Ϊԭ��ظ��������øõ�ص�ⱥ��ʳ��ˮ(���ص缫��Ϊ���Ե缫) 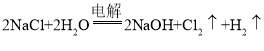 ����������������4480mL����(��״��)����ʱ���������ʵ���Ϊ0.2mol�������������������ʵ�����0.1mol������ݹ�ϵʽ
����������������4480mL����(��״��)����ʱ���������ʵ���Ϊ0.2mol�������������������ʵ�����0.1mol������ݹ�ϵʽ![]() ��֪������﮵�����Ϊ0.2mol��7g/mol��1.4g���ʴ�Ϊ��Li��1.4g��
��֪������﮵�����Ϊ0.2mol��7g/mol��1.4g���ʴ�Ϊ��Li��1.4g��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
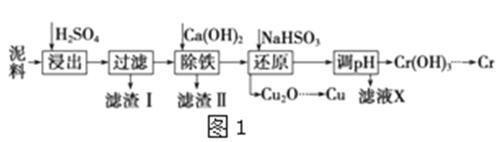
Сѧ��10����Ӧ����ϵ�д�����Ŀ����ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ�����ͭ���Ƚ���������������ͼ1��
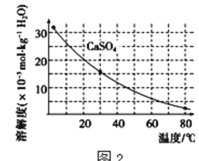
��֪�������ʳ�����pH��CaSO4���ܽ��������ͼ2��
Fe3+ | Cu2+ | Cr3+ | |
��ʼ����pH | 2.1 | 4.7 | 4.3 |
��ȫ����pH | 3.2 | 6.7 | a |
(1)�ڽ��������г�������Fe2(SO4)3��Cr2(SO4)3�⣬��Ҫ����__��
(2)�ڳ��������У���Ҫ��ȥFe3+��CaSO4���������ز�����������ʯ�������pH��Լ__������Fe3+�Ѿ������IJ�����__��������Һ�ӵ�80����__��
(3)д����ԭ�����м���NaHSO3����Cu2O���巴Ӧ�����ӷ���ʽ__���˲����м���NaHSO3�õ�Cu2O�IJ���Ϊ95%����NaHSO3�����������˷��Լ��⣬������ֵ�������__��
(4)��FeS������Һ�д��ڣ�FeS(s)![]() Fe2+(aq)+S2-(aq)��������FeS��Ksp=6.25��10-18����֪FeS������Һ��c(H+)��c(S2-)֮���������������ϵ��c2(H+)c(S2-)=1.0��10-22��Ϊ��ʹ��Һ��c(Fe2+)�ﵽ1molL-1���ֽ�����FeSͶ���䱥����Һ�У�Ӧ������Һ�е�c(H+)Ϊ___��
Fe2+(aq)+S2-(aq)��������FeS��Ksp=6.25��10-18����֪FeS������Һ��c(H+)��c(S2-)֮���������������ϵ��c2(H+)c(S2-)=1.0��10-22��Ϊ��ʹ��Һ��c(Fe2+)�ﵽ1molL-1���ֽ�����FeSͶ���䱥����Һ�У�Ӧ������Һ�е�c(H+)Ϊ___��