题目内容
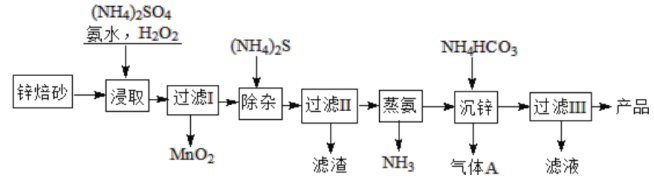
【题目】(加试题)NH4Al(SO4)2·12H2O(铵明矾)可用作泡沫灭火器的内留剂、石油脱色剂等。某兴趣小组同学用氧化铁、铝粉、镁条和氯酸钾等物质做铝热反应后的铝灰及硫酸铵等为原料制备铵明矾的实验,步骤如下:

(1)下列有关说法中正确的是_________。
A.“滤液1”中含有K+、Mg2+、Cl-
B.“滤渣1”和“滤渣2”中含有相同的物质
C.“过滤1”可用倾析法,以缩减实验时间
D.将“滤液3”蒸干并灼烧,可得纯碱
(2)用NaOH溶解“滤渣1”时,可以采用_________的方式提高浸出率(写出3条)。
(3)向“滤液2”中通入足量的CO2,写出相应的离子反应方程式__________________。
(4)由“滤渣3”制备铵明矾,经过如下步骤:a→g→_________→h(依次填入正确的序号)
a.加硫酸溶解 b.抽滤
c.加入蒸发皿中
d.降温结晶
e.蒸发至表面出现晶膜
f.配制饱和硫酸铵溶液
g.将硫酸铝溶液转移至蒸发皿
h.洗涤、干燥
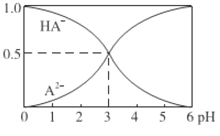
(5)①根据各物质的溶解度曲线(见下图),在80℃时,用一定浓度的硫酸溶解“滤渣3”时,最适宜的硫酸浓度为_________。

A.3mol/L(1.20g/mL)
B.6mol/L(1.34g/mL)
C.9mol/L(1.49 g/mL)
D.18mol/L (1.84g/mL)
②所需硫酸用量的简便确定方法是__________________。
【答案】BD 加热、提高NaOH浓度、搅拌等 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- OH-+CO2=HCO3- f→c→e→d→b A 逐滴加入(3 mo1·L-1)硫酸,并不断搅拌,至沉淀恰好完全溶解
【解析】
铝灰水洗的目的是洗去表面的氯酸钾杂质,所以滤液1主要含有KClO3,滤渣1主要含有氧化铁、铝粉、镁条,加入NaOH溶液,Al与NaOH溶液反应生成偏铝酸钠,故滤液2中主要含有偏铝酸钠和氢氧化钠,滤渣2中主要含有氧化铁、镁条,向滤液2中通入CO2气体,偏铝酸钠与CO2反应生成氢氧化铝,故滤渣3为氢氧化铝,得到的氢氧化铝再制备NH4Al(SO4)2·12H2O(铵明矾),据此答题。
(1)A.“滤液1”中主要含有氯酸钾,故含有K+、ClO3-,故A错误;
B.“滤渣1”中含有氧化铁、铝粉、镁条,“滤渣2”中含有氧化铁、镁条,含有相同的物质为氧化铁、镁条,故B正确;
C.倾析法可以将颗粒较大的固体与溶液分离,滤渣1中含有铝粉,颗粒较小,不能使用倾析法,故C错误;
D.“滤液3”中主要含有碳酸氢钠,碳酸氢钠蒸干并灼烧,受热分解生成纯碱,故D正确。
故答案为:BD。
(2)用NaOH溶解“滤渣1”时,可采用加热、提高NaOH浓度、搅拌等方式提高浸出率,故答案为:加热、提高NaOH浓度、搅拌等。
(3)向“滤液2”中通入足量的CO2,偏铝酸钠与CO2反应生成氢氧化铝和碳酸氢钠,氢氧化钠与足量的CO2反应生成碳酸氢钠,离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- OH-+CO2=HCO3-,故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- OH-+CO2=HCO3-。
(4)由“滤渣3”中主要含有氢氧化铝,先加硫酸溶解,氢氧化铝与硫酸反应生成硫酸铝和水,将硫酸铝溶液转移至蒸发皿中,配制饱和硫酸铵溶液,加入蒸发皿中,蒸发至表面出现晶膜,降温结晶,抽滤,得到铵明矾,洗涤、干燥。所以制备铵明矾的步骤为:a→g→f→c→e→d→b→h,故答案为:f→c→e→d→b。
(5)①由图可知,80℃时Al2(SO4)318H2O的溶解度约为70g,则100g水中可溶解70g晶体,则n[Al2(SO4)318H2O]=70g/666g/mol≈0.1mol,n(H2SO4)=n(SO42-)=0.1mol×3=0.3mol,若H2SO4溶解Al2O3后溶液的体积变化忽略不计,则c(H2SO4)=0.3mol/0.1L=3mol/L,故答案为:A。
②用3mol/L的H2SO4溶解Al2O3后,得到的溶液接近Al2(SO4)318H2O的饱和溶液,有利于铵明矾的制备(可减少蒸发水的量),故答案为:逐滴加入(3 mo1·L-1)硫酸,并不断搅拌,至沉淀恰好完全溶解。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案