题目内容
下列物质的工业制备原理的方程式书写正确的是
A.氢氧化钠:Na2CO3+Ca(OH)2 CaCO3↓+2NaOH CaCO3↓+2NaOH |
B.乙醇:C6H12O6 2C2H5OH+2CO2↑ 2C2H5OH+2CO2↑ |
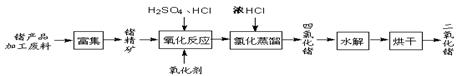
C.二氧化硫:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O |
D.氯气:Ca(ClO)2+4HCl(浓) CaCl2+2Cl2↑+2H2O CaCl2+2Cl2↑+2H2O |
B
解析试题分析:A.NaOH在工业上用电解饱和食盐水的方法制取。方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH。错误。B符合制取方法,方程式书写无误。C.在工业上SO2是用煅烧黄铁矿的方法制取的。方程式为4FeS2+11O2
Cl2↑+H2↑+2NaOH。错误。B符合制取方法,方程式书写无误。C.在工业上SO2是用煅烧黄铁矿的方法制取的。方程式为4FeS2+11O2 2Fe2O3+8SO2↑.错误。D.在工业常用电解饱和食盐水的方法制氯气。方程式为2NaCl+2H2O
2Fe2O3+8SO2↑.错误。D.在工业常用电解饱和食盐水的方法制氯气。方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH。错误。
Cl2↑+H2↑+2NaOH。错误。
考点:考查物质的工业制法的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下: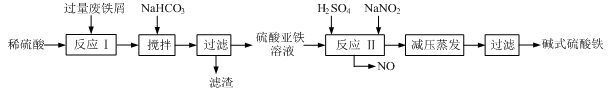
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入过量废铁屑的目的是 ,此时溶液中存在的阳离子主要有 ,用NaHCO3调整溶液pH时的离子方程式是 。
(2)在实际生产中,反应Ⅱ中常同时通入O2以减少NaNO2的用量,同时通入O2的作用是 。
(3)碱式硫酸铁溶于水后能电离产生[Fe(OH)]2+离子,写出[Fe(OH)]2+发生水解反应生成Fe(OH)3的离子方程式 。
(4)已知废铁屑中铁元素的质量分数为84.0%,若不考虑每步反应中铁元素的损耗,现有100吨废铁屑理论上最多能生产 吨碱式硫酸铁。
尿素是第一个人工合成的有机物,下列关于尿素的叙述不正确的是 ( )。
| A.尿素是一种氮肥 |
| B.尿素是人体新陈代谢的一种产物 |
| C.尿素能发生水解反应 |
| D.尿素是一种酸性物质 |
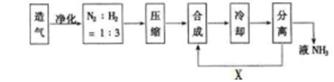
对于可逆反应N2(g)+3H2(g) 2NH3(g) ΔH<0,下列说法正确的是( )。
2NH3(g) ΔH<0,下列说法正确的是( )。
| A.达到平衡时反应物和生成物浓度一定相等 |
| B.达到平衡后加入氨气,重新达到平衡时,氨气的浓度比原平衡时大 |
| C.达到平衡时,升高温度加快了吸热反应的速率,降低了放热反应的速率,所以平衡向逆反应的方向移动 |
| D.加入催化剂可以缩短到达平衡的时间,这是因为加快了正反应的速率,而减慢了逆反应的速率 |
如图所示是一种综合处理SO2废气的工艺流程,若每步都完全反应。下列说法正确的是 ( )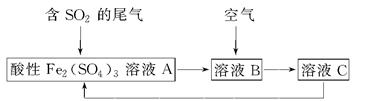
| A.溶液B中发生的反应为2SO2+O2=2SO3 |
| B.可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+ |
| C.由以上流程可推知氧化性:Fe3+>O2>SO42— |
| D.此工艺的优点之一是物质能循环利用 |
下列叙述中不属于土壤酸化原因的是( )。
| A.土壤胶体吸附的H+、Al3+被其他阳离子交换 |
| B.微生物、细菌在利用土壤中的有机物时,会产生二氧化碳和多种有机酸 |
| C.微生物、细菌在利用土壤中物质时,将土壤中的NH3转化为亚硝酸和硝酸,将硫化物转化为硫酸 |
| D.土壤有机物中的氮被微生物分解生成氨的氨化过程,会使土壤的pH升高 |