��Ŀ����
����Ŀ�������£���20mL ��Һ����ȡ��ˮ����ƿ�У���0.05moL/LHCl��Һ�ζ�����pH�Ʋɼ����ݣ����Ի��Ƶĵζ���������ͼ��ʾ������˵����ȷ����
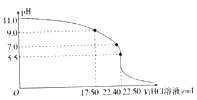
A. ��pH=11.0ʱ��NH3H2O�ĵ���ƽ�ⳣ��Kb=1.78��10-5
B. ��pH=9.0 ʱ��c(Cl-)>c(NH4+ )>c(OH-) >c(H+)
C. ��pH= 5.5ʱ����Һ����5 ����
D. ��pH= 7.0 ʱ����ˮ��HCl ��Һǡ����ȫ��Ӧ
���𰸡�A
��������A��谱ˮ���ʵ���Ũ��Ϊxmol/L��pH=11.0ʱc��OH-��=c��NH4+��=1![]() 10-3mol/L����ʱc��NH3��H2O��=xmol/L-c��NH4+��
10-3mol/L����ʱc��NH3��H2O��=xmol/L-c��NH4+��![]() xmol/L�����ݵ���ƽ�ⳣ���ĸ���ó���c��OH-����c��NH4+��=Kb��c��NH3��H2O����1
xmol/L�����ݵ���ƽ�ⳣ���ĸ���ó���c��OH-����c��NH4+��=Kb��c��NH3��H2O����1![]() 10-3
10-3![]() 1
1![]() 10-3=Kbx����ʽ����pH=7.0ʱ����22.40mLHCl����ʱ��Һ�еĵ���غ�Ϊc��NH4+��+c��H+��=c��OH-��+c��Cl-����pH=7.0��c��H+��=c��OH-��=1
10-3=Kbx����ʽ����pH=7.0ʱ����22.40mLHCl����ʱ��Һ�еĵ���غ�Ϊc��NH4+��+c��H+��=c��OH-��+c��Cl-����pH=7.0��c��H+��=c��OH-��=1![]() 10-7mol/L����c��NH4+��=c��Cl-��=
10-7mol/L����c��NH4+��=c��Cl-��=![]() mol/L�����������غ��ʱc��NH3��H2O��=��
mol/L�����������غ��ʱc��NH3��H2O��=��![]() -
-![]() ��mol/L=
��mol/L=![]() mol/L�����ݵ���ƽ�ⳣ��ֻ���¶��йأ���Ũ���أ�1
mol/L�����ݵ���ƽ�ⳣ��ֻ���¶��йأ���Ũ���أ�1![]() 10-7
10-7![]() =Kb
=Kb![]() ����ʽ����������ʽ����ʽ���x=0.05632��Kb=1.78
����ʽ����������ʽ����ʽ���x=0.05632��Kb=1.78![]() 10-5��A����ȷ��B������������Һ��һ�����ڵ���غ�c��NH4+��+c��H+��=c��OH-��+c��Cl-����pH=9.0ʱc��OH-��
10-5��A����ȷ��B������������Һ��һ�����ڵ���غ�c��NH4+��+c��H+��=c��OH-��+c��Cl-����pH=9.0ʱc��OH-��![]() c��H+������c��Cl-��
c��H+������c��Cl-��![]() c��NH4+����B�����C�pH=5.5ʱ����Һ�д��ڵ�����NH4+��Cl-��H+��OH-��NH3��H2O��H2O��C�����D���ˮ������ǡ����ȫ��Ӧ����NH4Cl��NH4Cl����ǿ�������Σ�NH4Cl��Һ�����ԣ�pH=7.0ʱ��ˮ������D�����ѡA��
c��NH4+����B�����C�pH=5.5ʱ����Һ�д��ڵ�����NH4+��Cl-��H+��OH-��NH3��H2O��H2O��C�����D���ˮ������ǡ����ȫ��Ӧ����NH4Cl��NH4Cl����ǿ�������Σ�NH4Cl��Һ�����ԣ�pH=7.0ʱ��ˮ������D�����ѡA��

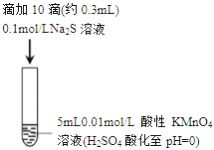
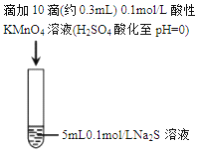
����Ŀ��ijС���о�Na2S ��Һ��KMnO4��Һ��Ӧ��̽����������
ʵ����� | I | II |
ʵ����� |
|
|
ʵ������ | ��ɫ��dz��pH | ��Һ�ʵ���ɫ��pH |
����: i.MnO4-��ǿ���������±���ԭΪMn2+���ڽ����������±���ԭΪMnO2
ii.�����������������Һ����Һ�ʵ���ɫ��
����˵����ȷ����
A. ����ʵ���֪��Na2S����ԭ
B. ȡʵ��I��������Һ����ʵ�飬����SO42-���ó�S2-��������SO42-
C. ʵ��I�з�Ӧ���ӷ���ʽ: 2MnO4-+3Mn2++2H2O=5MnO2��+4H+
D. ʵ��II �з�Ӧ��������Һ�ʵ���ɫ����MnO2����
����Ŀ��ʵ������������������Ҫװ����ͼA��ʾ����Ҫ�������a�Թ��а�2��3��2�����������Ũ���ᡢ�Ҵ�������Ļ����ڰ�Aͼ����װ�ã�ʹ����������������ͨ��b�Թ���ʢ�ı���̼������Һ(���뼸�η�̪��Һ)�У���С�����a�Թ��еĻ��Һ���ܵ�b�Թ����ռ���Լ2 mL����ʱֹͣ���ȡ�����b�Թܲ�������Ȼ���ô�����Һ��ֲ㣻�ݷ��������������������

��ش��������⣺
(1) ������пɹ۲쵽b�Թ�����ϸС������ð����д���÷�Ӧ�����ӷ���ʽ��___��
(2) Aװ����ʹ�����ιܳ������������⣬��һ��Ҫ������___��������з���������������ʹ�õ�һ��������___��
(3) Ϊ֤��Ũ�����ڸ÷�Ӧ�����˴�������ˮ�������ã�ijͬѧ������ͼA��ʾװ�ý���������4��ʵ�顣ʵ�鿪ʼ���þƾ�����3min���ټ���ʹ֮����3min��ʵ�����������С�Թ�b�ٲ��л���ĺ�ȣ�ʵ���¼���£�
ʵ�� ��� | �Թ�a���Լ� | �Թ�b���Լ� | ����л���ĺ��/cm |
A | 3 mL�Ҵ���2 mL���ᡢ1mL 18mol��L-1Ũ���� | ����Na2CO3��Һ | 5.0 |
B | 3 mL�Ҵ���2 mL���� | 0.1 | |
C | 3 mL�Ҵ���2 mL���ᡢ6 mL 3mol��L-1H2SO4 | 1.2 | |
D | 3 mL�Ҵ���2 mL���ᡢ���� | 1.2 |
��ʵ��D��Ŀ������ʵ��C����գ�֤��H+��������Ӧ���д����á�ʵ��D��Ӧ��������������Ũ�ȷֱ���__mL��___mol��L-1��
�ڷ���ʵ��___(��ʵ����)�����ݣ������Ʋ��ŨH2SO4����ˮ����������������IJ��ʡ�Ũ�������ˮ���ܹ���������������ʵ�ԭ����___��
�ۼ���������������������IJ��ʣ���ʵ�鷢���¶ȹ������������IJ��ʷ������ͣ����ܵ�ԭ����___��
�ܷ�����������������ϴ�ӣ�Ϊ�˸�������������ѡ�õĸ����Ϊ__ (����ĸ)��
A.P2O5B.��ˮNa2SO4C.��ʯ��D.NaOH����