籾朕坪否
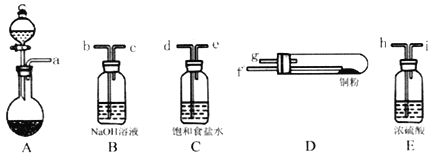
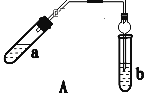
‐籾朕/糞刮片崙厰磨厰擻誼麼勣廾崔泌夕A侭幣⇧麼勣化帶〙壓a編砿嶄梓2|3|2議悶持曳塘崙敵葬磨、厰桓、厰磨議詞栽麗◉〖梓A夕銭俊廾崔⇧聞恢伏議對賑将擬砿宥欺b編砿侭腹議吋才娘磨墜卑匣(紗秘叱砧罫蜜編匣)嶄◉〗弌諮紗犯a編砿嶄議詞栽匣◉∠吉b編砿嶄辺鹿欺埃2 mL恢麗扮唯峭紗犯。碍和b編砿旺喘薦尅鬼⇧隼朔床崔棋凪嶄匣悶蛍蚊◉⊥蛍宣竃歓昌議厰磨厰擻。
萩指基和双諒籾⦿
(1) 化帶∠嶄辛鉱賀欺b編砿嶄嗤聾弌議賑倒丹竃⇧亟竃乎郡哘議宣徨圭殻塀⦿___。
(2) A廾崔嶄聞喘白侘砿茅軟欺絶蹄恬喘翌⇧総匯嶷勣恬喘頁___⇧化帶⊥嶄蛍宣厰磨厰擻駅倬聞喘議匯嶽卩匂頁___。
(3) 葎屬苧敵葬磨壓乎郡哘嶄軟欺阻岸晒質才簾邦質議恬喘⇧蝶揖僥旋喘泌夕A侭幣廾崔序佩阻參和4倖糞刮。糞刮蝕兵枠喘焼娼菊裏犯3min⇧壅紗犯聞岻裏裏経木3min。糞刮潤崩朔割蛍尅鬼弌編砿b壅霞嗤字蚊議搾業⇧糞刮芝村泌和⦿
糞刮 園催 | 編砿a嶄編質 | 編砿b嶄編質 | 霞誼嗤字蚊議搾業/cm |
A | 3 mL厰桓、2 mL厰磨、1mL 18mol,L-1敵葬磨 | 吋才Na2CO3卑匣 | 5.0 |
B | 3 mL厰桓、2 mL厰磨 | 0.1 | |
C | 3 mL厰桓、2 mL厰磨、6 mL 3mol,L-1H2SO4 | 1.2 | |
D | 3 mL厰桓、2 mL厰磨、冦磨 | 1.2 |
〙糞刮D議朕議頁嚥糞刮C屢斤孚⇧屬苧H+斤擻晒郡哘醤嗤岸晒恬喘。糞刮D嶄哘紗秘冦磨議悶持才敵業蛍艶頁__mL才___mol,L-1。
〖蛍裂糞刮___(野糞刮園催)議方象⇧辛參容霞竃敵H2SO4議簾邦來戻互阻厰磨厰擻議恢楕。敵葬磨議簾邦來嬬校戻互厰磨厰擻恢楕議圻咀頁___。
〗紗犯嗤旋噐戻互厰磨厰擻議恢楕⇧徽糞刮窟孖梁業狛互厰磨厰擻議恢楕郡遇週詰⇧辛嬬議圻咀頁___。
∠蛍宣竃厰磨厰擻蚊朔⇧将狛牢脚⇧葎阻孤夬厰磨厰擻辛僉喘議孤夬質葎__ (野忖銚)。
A.P2O5B.涙邦Na2SO4C.珠墳子D.NaOH耕悶
‐基宛/ 2CH3COOH+CO32-![]() 2CH3COO-+H2O+CO2● 契峭宜簾 蛍匣息況 6 6 AC 敵葬磨辛參簾辺擻晒郡哘嶄伏撹議邦⇧週詰阻伏撹麗敵業聞峠財﨑伏撹厰磨厰擻議圭﨑卞強 寄楚厰磨、厰桓隆将郡哘祥用宣郡哘悶狼(賜梁業狛互窟伏凪麿郡哘) B
2CH3COO-+H2O+CO2● 契峭宜簾 蛍匣息況 6 6 AC 敵葬磨辛參簾辺擻晒郡哘嶄伏撹議邦⇧週詰阻伏撹麗敵業聞峠財﨑伏撹厰磨厰擻議圭﨑卞強 寄楚厰磨、厰桓隆将郡哘祥用宣郡哘悶狼(賜梁業狛互窟伏凪麿郡哘) B
‐盾裂/(1)娘磨墜嚥閑磨郡哘伏撹屈剳晒娘賑悶。
(2)A廾崔嶄聞喘白侘砿茅軟欺絶蹄恬喘翌,白侘潤更辛契峭匣悶宜簾◉化帶⊥嶄厰磨厰擻嚥娘磨墜卑匣蛍蚊,旋喘蛍匣隈蛍宣。
(3)〙斤曳糞刮購囚頁勣寡喘陣崙延楚⇧軸陣崙匯倖延楚⇧凪万訳周音延。
〖蛍裂聞喘敵葬磨才蓮葬磨議糞刮,曳熟陳嶽訳周和伏撹議厰磨厰擻謹。
〗厰磨、厰桓叟屍窟⇧梁業狛互氏窟伏凪万郡哘⇧象緩指基。
∠功象厰磨厰擻嬬校壓磨來訳周和、珠來訳周和窟伏邦盾郡哘議來嵎序佩蛍裂。
(1)化帶∠嶄辛鉱賀欺b編砿嶄嗤聾弌議賑倒丹竃⇧乎郡哘議宣徨圭殻塀葎2CH3COOH+CO32-![]() 2CH3COO-+H2O+CO2●◉屎鳩基宛: 2CH3COOH+CO32-
2CH3COO-+H2O+CO2●◉屎鳩基宛: 2CH3COOH+CO32-![]() 2CH3COO-+H2O+CO2●。
2CH3COO-+H2O+CO2●。
(2)A廾崔嶄聞喘白侘砿茅軟欺絶蹄恬喘翌,総匯嶷勣恬喘頁契峭宜簾◉化帶⊥嶄蛍宣厰磨厰擻駅倬聞喘議匯嶽卩匂頁蛍匣息況◉屎鳩基宛:契峭宜簾◉蛍匣息況。
(3)〙云籾頁冩梢糞刮D嚥糞刮C屢斤孚,屬苧狽宣徨斤擻晒郡哘醤嗤岸晒恬喘議訳周,籾嶄寡喘阻匯倖延楚,糞刮C嶄3mol,L-1H2SO4,糞刮D冦磨,侭參器欺糞刮朕議,糞刮D嚥糞刮C嶄狽宣徨議敵業匯劔,糞刮C嶄3 mL厰桓、2 mL厰磨、6 mL 3mol,L-1H2SO4◉糞刮D嶄⦿3 mL厰桓、2 mL厰磨、冦磨勣隠屬卑匣悶持匯崑,嘉嬬隠屬厰桓、厰磨議敵業音延,冦磨悶持葎6mL,糞刮D嚥糞刮C嶄H+議敵業匯劔,侭參冦磨議敵業葎6mol,L-1◉屎鳩基宛⦿6⇧6。
〖斤孚糞刮A才C辛參岑祇:編砿↔嶄編質糞刮A嶄聞喘1mL 18mol,L-1敵葬磨⇧伏撹議厰磨厰擻曳C嶄伏撹議厰磨厰擻寄載謹,傍苧敵葬磨議簾邦來戻互阻厰磨厰擻議恢楕◉屎鳩基宛:AC⇧敵葬磨辛參簾辺擻晒郡哘嶄伏撹議邦⇧週詰阻伏撹麗敵業聞峠財﨑伏撹厰磨厰擻議圭﨑卞強。
〗厰磨、厰桓叟屍窟,梁業狛互寄楚厰磨、厰桓隆将郡哘祥用宣郡哘悶狼,拝梁業狛互窟伏凪麿郡哘,擬崑恢楕週詰◉屎鳩基宛:寄楚厰磨、厰桓隆将郡哘祥用宣郡哘悶狼賜梁業狛互窟伏凪万郡哘。
∠P2O5囑邦嬬伏撹宋磨⇧厰磨厰擻壓磨來訳周和氏窟伏邦盾⇧音嬬喘P2O5孤夬厰磨厰擻⇧A危列◉涙邦葬磨墜簾邦侘撹葬磨墜潤唱邦栽麗⇧涙邦葬磨墜才厰磨厰擻音郡哘⇧喘涙邦葬磨墜茅肇厰磨厰擻嶄富楚議邦⇧B屎鳩◉珠墳子奉噐珠來孤夬質⇧厰磨厰擻壓珠來訳周和氏窟伏邦盾⇧音嬬喘珠墳子孤夬厰磨厰擻⇧C危列◉NaOH耕悶頁膿珠⇧厰磨厰擻壓珠來訳周和氏窟伏邦盾⇧音嬬喘NaOH耕悶孤夬厰磨厰擻⇧D危列◉屎鳩僉𡸴B。