题目内容
17.某粗碘样品中含有氯化碘(ICl)和溴化碘(IBr),它们的性质和卤素单质相似,利用碘的升华提纯碘之前,要加适量的某物质对粗碘进行预处理,加入的物质可能是( )| A. | 碘化钾 | B. | 硝酸银 | C. | 溴化钠 | D. | 液氯 |
分析 利用碘易升华的特性精制碘,须使ICl、IBr中的Cl、Br变为难挥发性的物质,而使其中的+1价的碘被还原为I2,同时加入的物质和碘(I2)不反应.
解答 解:A.加入KI发生:反应为IBr+KI=I2+KBr,ICl+KI=I2+KCl,加热时I2升华与KCl、KBr分离,故A正确;
B.加入硝酸银,硝酸银和IBr、ICl反应生成AgCl、AgBr和HIO,不能达到提纯碘的目的,故B错误;
C.加入NaBr,IBr和NaBr不反应,不能达到除杂目的,故C错误;
D.液氯和IBr不反应,不能达到除杂目的,故D错误;
故选A.
点评 本题考查卤族元素性质,为高频考点,侧重考查学生获取信息的自学能力,采用知识迁移的方法分析解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7. 某温度下,在体积为1L的密闭容器中,存在如下关系:xHF(g)?(HF)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法错误的是( )
某温度下,在体积为1L的密闭容器中,存在如下关系:xHF(g)?(HF)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法错误的是( )
 某温度下,在体积为1L的密闭容器中,存在如下关系:xHF(g)?(HF)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法错误的是( )
某温度下,在体积为1L的密闭容器中,存在如下关系:xHF(g)?(HF)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法错误的是( )| A. | x=2 | |
| B. | 平衡时混合气体的平均摩尔质量是23.3g/mol | |
| C. | 该温度下,反应的平衡常数为0.25 L•mol-1 | |
| D. | t1时刻,保持恒温恒容,再充入1mol HF(g),重新达到平衡时,$\frac{c[(HF)_{x}]}{c(HF)}$增大 |
8.a g KNO3溶于b g水,形成V mL饱和溶液.下列关系式错误的是( )
| A. | KNO3物质的量浓度:c(KNO3)=$\frac{a}{101V}$mol•L-1 | |
| B. | 20℃时KNO3的溶解度S=$\frac{100a}{b}$ g | |
| C. | KNO3质量分数:w(KNO3)=$\frac{100a}{a+b}$% | |
| D. | 该溶液的密度ρ=$\frac{1000(a+b)}{V}$g•L-1 |
17.锌锰废电池可回收锌、锰元素生产硫酸锌及碳酸锰,其中生产碳酸锰的主要工艺如下:
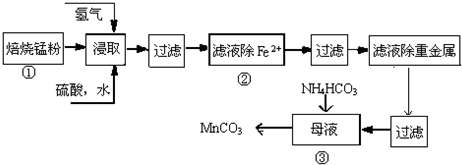
试回答下列问题:
(1)硫酸锌水溶液显酸性,用离子方程式说明Zn2++2H2O?Zn(OH)2+2H+.
(2)原料锰粉粗品中主要成分为MnO2和炭,在过程①焙烧时反应的化学方程式为MnO2+C═MnO+CO↑,该反应的氧化产物是CO,每生成44.8L(标准状况下)气体时转移电子数为4NA.
(3)在50~55℃时向过程③中MnSO4的母液中加入足量NH4HCO3,有气体生成,其化学方程式为:MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+H2O+CO2↑.
(4)已知三种离子沉淀的pH范围为Fe3+:2.7~3.7. Mn2+:8.6~10.1,Fe2+:7.6~9.6.下表是上述过程②中除去Fe2+的模拟操作方法,请完成下表内容:

试回答下列问题:
(1)硫酸锌水溶液显酸性,用离子方程式说明Zn2++2H2O?Zn(OH)2+2H+.
(2)原料锰粉粗品中主要成分为MnO2和炭,在过程①焙烧时反应的化学方程式为MnO2+C═MnO+CO↑,该反应的氧化产物是CO,每生成44.8L(标准状况下)气体时转移电子数为4NA.
(3)在50~55℃时向过程③中MnSO4的母液中加入足量NH4HCO3,有气体生成,其化学方程式为:MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+H2O+CO2↑.
(4)已知三种离子沉淀的pH范围为Fe3+:2.7~3.7. Mn2+:8.6~10.1,Fe2+:7.6~9.6.下表是上述过程②中除去Fe2+的模拟操作方法,请完成下表内容:
| 实验操作 | 离子方程式 |
| 步骤1:取少量滤液于试管中,加入过量酸化的H2O2溶液,振荡. | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| 步骤2:将pH调到3.7~8.6,使Fe3+沉淀完全. | Fe3++3H2O?Fe(OH)3+3H+ |