题目内容
2.现有下列有机物:A.C2H50H;B.C6H50H;C.CH2=CH-CH3; D.葡萄糖; E淀粉; F.蔗糖; G.麦芽糖;H.CH3COOCH3
(1)能用来杀菌的是A(填字母代号,下同).
(2)能与Na0H溶液反应的是BH
(3)常温下能和溴水反应的是C
(4)能和银氨溶液反应的是DG
(5)在一定条件下能形成高分子化合物的是C
(6)能水解最终生成一种有机物的是EG.
分析 (1)75%的乙醇具有良好的杀菌消毒效果;
(2)酸和酯类物质能够与氢氧化钠溶液反应;
(3)含有碳碳双键的有机物能够与溴水发生加成反应;
(4)有机物分子中含有醛基时能够发生银镜反应;
(5)含有碳碳双键、碳碳三键的有机物能够形成高分子化合物;
(6)淀粉最终水解生成葡萄糖,麦芽糖水解生成葡萄糖.
解答 解:(1)乙醇能够使蛋白质变性,能用来杀菌,
故答案为:A;
(2)A.C2H50H、H.CH3COOCH3能与Na0H溶液反应,
故答案为:BH;
(3)C.CH2=CH-CH3中含有碳碳双键,常温下能和溴水发生加成反应,
故答案为:C;
(4)含有醛基的有机物能和银氨溶液发生银镜反应,如:D.葡萄糖、G.麦芽糖,
故答案为:DG;
(5)C.CH2=CH-CH3含有碳碳双键,在一定条件下能形成高分子化合物,
故答案为:C;
(6)E淀粉最终水解产物为葡萄糖,G.麦芽糖水解生成2分子葡萄糖,所以能水解最终生成一种有机物的是EG,
故答案为:E G.
点评 本题考查了常见有机物结构与性质,题目难度中等,明确常见官能团结构及具有的性质为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
12.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第三周期VI族,Y和Z的最高价氧化物对应的水化物的酸性较强的是HClO4(写化学式).
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键,X的杂化轨道类型是sp,XY2的分子的空间构形为直线形.在H-Y、H-Z两种共价键中,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.
已知:
XO(g)+0.5O2(g)=XO2(g)△H=-283.0kJ/mol
Y(g)+O2(g)=YO2(g)△H=-296.0kJ/mol
此反应的热化学方程式是2CO(g)+SO2(g)=2CO2(g)+S(g)△H=-270kJ/mol.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键,X的杂化轨道类型是sp,XY2的分子的空间构形为直线形.在H-Y、H-Z两种共价键中,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.
已知:
XO(g)+0.5O2(g)=XO2(g)△H=-283.0kJ/mol
Y(g)+O2(g)=YO2(g)△H=-296.0kJ/mol
此反应的热化学方程式是2CO(g)+SO2(g)=2CO2(g)+S(g)△H=-270kJ/mol.
13.下列说法正确的是( )
| A. | 用玻璃棒蘸取某未知溶液进行焰色反应,若火焰颜色为黄色则说明一定有钠元素 | |
| B. | 某未知溶液加稀氢氧化钠溶液,未产生能使湿润红色石蕊试纸变蓝的气体,则说明原溶液不含NH${\;}_{4}^{+}$ | |
| C. | 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| D. | 某溶液加入盐酸,无明显现象,再加BaCl2溶液,产生白色沉淀,则说明溶液中一定有 SO${\;}_{4}^{2-}$ |
17.某粗碘样品中含有氯化碘(ICl)和溴化碘(IBr),它们的性质和卤素单质相似,利用碘的升华提纯碘之前,要加适量的某物质对粗碘进行预处理,加入的物质可能是( )
| A. | 碘化钾 | B. | 硝酸银 | C. | 溴化钠 | D. | 液氯 |
7.下列有关原子的表示方法中正确的是( )
| A. | 中子数为16的磷原子:${\;}_{15}^{31}$P | |
| B. | 质子数为17的氯原子:${\;}_{17}^{35}$Cl | |
| C. | 质量数为57的铁原子:${\;}_{57}^{26}$Fe | |
| D. | 核外电子数为16的硫原子:${\;}_{16}^{32}$S |
5.氮化硅的强度很高,尤其是热压氮化硅,是世界上最坚硬的物质之一,氮化硅陶瓷可做燃气轮机的燃烧室、机械密封环、输送铝液的电磁泵的管道及阀门、永久性模具、钢水分离环等.制备氮化硅可将硅粉放在氮气中加热至1000℃左右直接氮化制得,实验室制备氮化硅装置示意图如图1:

回答下列问题:
(1)检查装置气密性的方法是在仪器D的出气口连接导管,将导管的末端插入水槽中的水中,用酒精灯轻轻加热圆底烧瓶,若导管口有气泡冒出且停止加热后,在导管中形成一段水柱,说明装置气密性良好,a仪器的名称是分液漏斗
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O;
(3)装置B的作用是除去氧气(及氮氧化物),装置C的作用是除去水蒸气;
(4)已知氮化硅的化学性质稳定,但常温下易溶于氢氟酸溶液生成一种白色的胶状沉淀和一种盐,请写出此化学反应方程式:Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F;
(5)实验室中某些气体的制取、收集及尾气处理装置如图2所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D

回答下列问题:
(1)检查装置气密性的方法是在仪器D的出气口连接导管,将导管的末端插入水槽中的水中,用酒精灯轻轻加热圆底烧瓶,若导管口有气泡冒出且停止加热后,在导管中形成一段水柱,说明装置气密性良好,a仪器的名称是分液漏斗
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O;
(3)装置B的作用是除去氧气(及氮氧化物),装置C的作用是除去水蒸气;
(4)已知氮化硅的化学性质稳定,但常温下易溶于氢氟酸溶液生成一种白色的胶状沉淀和一种盐,请写出此化学反应方程式:Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F;
(5)实验室中某些气体的制取、收集及尾气处理装置如图2所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D
| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Fe | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
2.CoCl2•6H2O在饲料、医药工业上有广泛的用途.下列是以含钴废料(含少量Fe、Al等杂质)为原料制取CoCl2•6H2O的一种新工艺流程如图1:
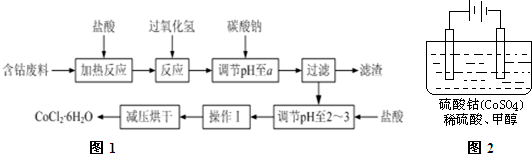
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(2)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(3)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(4)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少有毒气体的排放,防止大气污染、防止产品中混有硝酸盐.原工艺较新工艺也有优点,其主要优点是流程的步骤减小,工艺减化.
(5)含钴物质在工业上有重要用途,有一种电化学法除去甲醇的污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中甲醇氧化成CO2而净化.实验室用如图2装置模拟上述过程:
①写出阳极电极反应式Co2+-e-=Co3+.
②除去甲醇的离子反应为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,该过程中被氧化的元素是碳元素,当生产过程中产生标况下2.24LCO2时,共转移电子数为3.612×1023.

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7.5 | 7.6 | 3.8 |
| 完全沉淀 | 3.2 | 9.7 | 9.2 | 5.2 |
(1)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(2)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(3)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(4)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少有毒气体的排放,防止大气污染、防止产品中混有硝酸盐.原工艺较新工艺也有优点,其主要优点是流程的步骤减小,工艺减化.
(5)含钴物质在工业上有重要用途,有一种电化学法除去甲醇的污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中甲醇氧化成CO2而净化.实验室用如图2装置模拟上述过程:
①写出阳极电极反应式Co2+-e-=Co3+.
②除去甲醇的离子反应为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,该过程中被氧化的元素是碳元素,当生产过程中产生标况下2.24LCO2时,共转移电子数为3.612×1023.
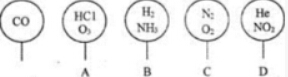 取五个相同的气球,同温同压下,分别充入CO和以下四种混合气体,吹出体积相等的状况,如图所示.A、B、C、D四个气球内,与CO所含原子数一定相等的是( )
取五个相同的气球,同温同压下,分别充入CO和以下四种混合气体,吹出体积相等的状况,如图所示.A、B、C、D四个气球内,与CO所含原子数一定相等的是( )