题目内容
下列化学反应的离子方程式不正确的是
| A.Na2S溶液中加入少量FeCl3溶液:2Fe3++S2- = 2Fe2++S↓ |
| B.向NaOH溶液中滴加碳酸氢钙溶液至OH-恰好完全反应:Ca2++2OH-+2HCO3- = CaCO3↓+2H2O+CO32- |
| C.向NaClO溶液中通入少量SO2气体:ClO-+SO2+H2O = SO42-+Cl-+2H+ |
D.Na2CO3溶液中滴入少量邻羟基苯甲酸溶液: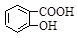 +CO32- +CO32- 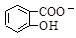 +HCO3- +HCO3- |
D
解析试题分析:A中氯化铁不足,所以生成氯化亚铁、单质S和氯化钠,A正确;B中当溶液至OH-恰好完全反应时,恰好生成碳酸钙、碳酸钠和水,B正确;次氯酸钠具有强氧化性,能把SO2氧化,C正确;选项D不正确,因为酚羟基也能和碳酸钠反应,答案选D。
考点:考查离子方程式的正误判断
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生能力的培养和训练。该题需要明确判断离子方程式正确与否的方法一般,即(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式,然后灵活运用即可。该题有助于培养学生分析问题、解决问题的能力。该题的难点在于生成物与反应物的用量有关系,需要讨论逐一分析、判断。

练习册系列答案
相关题目
下表对某些反应方程式的评价合理的是
| 编号 | 离子方程式或电极方程式 | 评价 | |
| A | Ca(ClO)2溶液中通入足量SO2 | Ca2++ClO-+SO2+H2O=CaSO4+Cl-+2H+ | 正确 |
| B | Ba(OH)2溶液中加入过量Al2(SO4)溶液 | 3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+Al(OH)3↓ | 正确 |
| C | 醋酸铵溶于水 | CH3COO-+NH4+ CH3COOH+NH3·H2O CH3COOH+NH3·H2O | 错误,阴阳离子水解相互促进,应该用“=”号 |
| D | 用惰性电极电解 CuCl2 和NaCl的混合溶液一段时间 | 阴极:Cu2++2e-=Cu 阳极:4OH—4e-=2H2O+O2 | 错误,只因为两级得失电子没配平 |
下列用来表示物质变化的化学反应中正确的是
| A.表示中和热的热化学方程式:H++OH-=H2O △H=-57.3kJ·mol-1 |
| B.硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH-=NH3↑+H2O |
| C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
| D.足量酸性高锰酸钾溶液与双氧水反应的离子方程式:2MnO4-+5H218O2+6H+=2Mn2++518O2↑+8H2O |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A.无色溶液:Ca2+、Fe3+、Cl-、NO3- |
| B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C.FeCl3溶液:K+、Na+、SO42-、AlO2- |
D. mol/L的溶液:Na+、K+、SiO32-、NO3- mol/L的溶液:Na+、K+、SiO32-、NO3- |
下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+ H2↑+ Cl2↑ H2↑+ Cl2↑ |
B.用银氨溶液检验乙醛中的醛基:CH3CHO +2Ag(NH3)2+ + 2OH-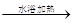 CH3COO- + NH4+ +3NH3 + 2Ag↓+ H2O CH3COO- + NH4+ +3NH3 + 2Ag↓+ H2O |
C.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32- 2C6H5OH + 2CO32- |
D.Na与乙醇反应:Na+CH3CH2OH CH3CH2ONa +H2↑ CH3CH2ONa +H2↑ |
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有 (填序号)。
①单质;②氧化物;③电解质;④盐;⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。

(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
| ①所有的离子方程式均可以表示一类反应 | |
| ②酸碱中和反应均可表示为H++OH-=H2O | |
| ③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号 | |
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO42-=BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
① ;
② ;
③ 。
 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下: