题目内容
(15分)某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
在圆底烧瓶中加入12.2 g苯甲酸和20 mL甲醇(密度约为0.79 g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
⑴浓硫酸的作用是________________________________________ _________;
若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式
___________________________________________________。
⑵甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲 酯的装置 (夹持仪器和加热仪器均已略去)。

根据有机物的沸点,最好采用______(填“甲”或“乙”)装置。
理由是______________________________________________。
⑶若要提高苯甲酸甲酯的产率,可采取的措施_
______ _。(任写一条)
Ⅱ.粗产品的精制
⑷苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称。

⑸通过计算,苯甲酸甲酯的产率为__________________________________。
(15分,除第二问第一空1分,其余均2分)(1)催化剂、吸水剂
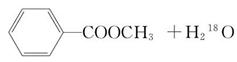
(2)甲 甲中有冷凝回流装置
(3)增加 CH3OH的用量
(4)分液 蒸馏
(5)65.0%
解析试题分析:(1)酯化反应在的浓硫酸起到了催化剂、吸水剂的作用;
根据酯化反应的原理,酸脱羟基醇脱氢,说明水中的羟基来自羧酸分子中,则表示反应前后18O位置的化学方程式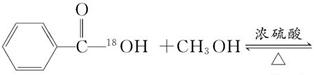
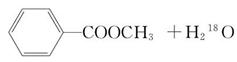
(2)根据有机物的沸点,最好采用甲装置;因为甲醇的沸点较低易挥发,甲中有冷凝回流装置,可以减少甲醇的损失;
(3)若要提高苯甲酸甲酯的产率,目的使平衡正向移动,可以增加 CH3OH或苯甲酸的用量,及时分离出产物;
(4)经过a步后得到水层和油层,所以a是分液;有机层又分离出不同的有机物,所以b是分馏;
(5)由所给数据可知甲醇过量,按苯甲酸的量计算,12.2g的苯甲酸的物质的量是0.1mol,理论上应得苯甲酸甲酯的质量是13.6g,实际得8.84g,所以苯甲酸甲酯的产率为8.84g/13.6g×100%=65.0%。
考点:考查醇与羧酸的酯化反应,实验原理、步骤、实验装置的判断,产率的计算

练习册系列答案
相关题目
将少量苯酚晶体溶入紫色石蕊试液中,石蕊试液呈现的颜色是
| A.紫色 | B.浅红 | C.蓝色 | D.无色 |
(7分)现有7瓶失去标签的液体,已知它们是有机试剂,可能是:①乙醇、②乙酸、③苯、④乙酸乙酯、⑤油脂、⑥葡萄糖溶液、⑦蔗糖溶液?现通过如下实验步骤来确定各试剂瓶中所装的液体:
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A?B?C?D?E?F?G后,闻气味 | 只有F?G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C?E?D三种液体不溶解而浮在水面上 |
| ③分别取少量7种液体于试管中加新制Cu(OH)2悬浊液并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
| ④各取少量C?E?D于试管中,加稀NaOH 溶液并加热 | 只有C仍有分层现象,且在D的试管中闻 到特殊香味 |
(1)试给它们的试剂瓶重新贴上标签,其中:
A____________, C____________, E________,F___________,G________?
(2)写出D与NaOH溶液的化学反应方程式: ____________________________
I.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为____________。
(2)下列物质中,不可以通过乙烯加成反应得到的是______(填序号)。
| A.CH3CH3 | B.CH3CHCl2 |
| C.CH3CH2OH | D.CH3CH2Br |
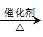 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
反应②的化学方程式为____________________________________。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________________,反应类型是__________________。
II.在实验室可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。

(1)乙醇、乙酸分子中官能团的名称分别是_________、_________。
(2)试管a中发生反应的化学方程式为
_____________________________________________,
反应类型是______________。
(3)浓H2SO4的作用是:__________________________。
反应开始前,试管b中盛放的溶液是____________。
该溶液的作用是
___________________________________________________________________________________。

 )该反应的原子利用率为100%,反应的化学方程式为___________。
)该反应的原子利用率为100%,反应的化学方程式为___________。

