题目内容
13. 制取氨气并完成喷泉实验(图中夹持装置均已略去).
制取氨气并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O
(2)收集氨气应使用向下排空气法法,要得到干燥的氨气可选用碱石灰做干燥剂.用湿润的红色石蕊试纸靠近集气瓶口看是否变蓝方法检验氨气是否已收集满.
(3)用左上图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是打开止水夹,挤出胶头滴管中的水.
分析 (1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气;
(2)氨气极易溶于水,密度比空气小,与浓盐酸反应生成氯化铵固体,有白烟生成,氨气水溶液呈碱性,可使石蕊试纸变蓝色;
(3)喷泉实验需形成明显的压力差.
解答 解:(1)实验室用加热氯化氨和消石灰的固体混合物制取氨气,方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O;
(2)氨气的密度比空气小,极易溶于水,只能用向下排气法收集,氨气为碱性气体,应用碱石灰干燥,氨气与浓盐酸反应生成氯化铵固体,有白烟生成,可用浓盐酸或湿润的红色石蕊试纸检验,根据生成白烟或集气瓶口是否变蓝判断是否收集满,
故答案为:向下排空气法;碱石灰;湿润的红色石蕊试纸靠近集气瓶口看是否变蓝;
(3)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:打开止水夹,挤出胶头滴管中的水.
点评 考查学生对元素化合物知识的熟悉程度.要求学生综合题中信息,结合对物质性质的了解,注意相关知识的积累,把握形成喷泉的实验条件以及对应物质的性质,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| B. | 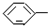 CH=CH 2是苯的同系物 CH=CH 2是苯的同系物 | |
| C. | 苯、油均不能使酸性KMnO4溶液褪色 | |
| D. | 人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用 |
4.在一定温度下某容积固定的密闭容器中,建立下列化学平衡:C(s)+H2O(g)?CO(g)+H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 体系的压强不再发生变化 | |
| B. | v正(CO)=v逆(H2O) | |
| C. | 生成nmolCO的同时生成nmolH2 | |
| D. | 1molH-H键断裂的同时断裂2molH-O键 |
8.现有A、B、C、D四种金属片,
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C.
根据上述情况判断四种金属的活泼由强到弱的顺序为( )
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C.
根据上述情况判断四种金属的活泼由强到弱的顺序为( )
| A. | DCAB | B. | CBAD | C. | BADC | D. | BACD |
18.下列说法正确的是( )
| A. | 油脂都能发生皂化反应 | B. | 用裂化汽油来萃取溴水中的溴 | ||
| C. | 糖属于高分子化合物 | D. | 油脂属于高分子化合物 |
5.下列各组离子在指定的溶液中一定能大量共存的是( )
| A. | 由水电离出的c (OH-)=10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、Br- | |
| B. | c(H+)/c(OH-)=1012的溶液中:Fe2+、Al3+、NO3-、Cl- | |
| C. | 含大量Al3+的溶液中:K+、Na+、SO42-、AlO2- | |
| D. | 无色溶液中:K+、Na+、MnO4-、SO42- |
3.下列说法中正确的是( )
| A. | 非自发反应一定不能实现 | |
| B. | 自发反应在任何条件下都能实现 | |
| C. | 同种物质气态时熵值最大,固态时熵值最小 | |
| D. | 放热同时熵减的反应高温下才能自发进行 |
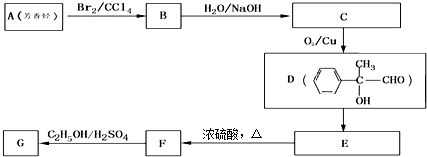
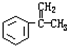
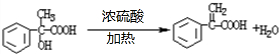 .③写出所有符合下列条件的F的同分异构体的结构简式:
.③写出所有符合下列条件的F的同分异构体的结构简式: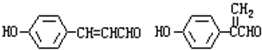 .
.