题目内容
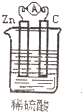
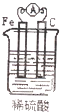
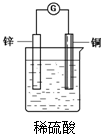
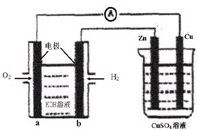
电浮选凝聚法处理酸性污水的工作原理如图所示.下列说法不正确的是( )
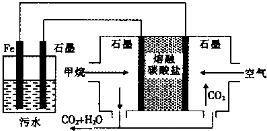

| A.铁电极的电极反应式为:Fe-2e-═Fe2+ |
| B.通人空气的石墨电极的电极反应式为O2+2CO2+4e-═2CO32- |
| C.若左池石墨电极产生44.8L(标准状况)气体,则消耗氧气0.5mol |
| D.为增强污水的导电能力,可向污水中加入适量工业用食盐 |
A.通入氧气的电极上得电子发生还原反应,所以通入氧气的电极为正极,则铁作阳极,阳极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,故A正确;
B.通入空气的电极为正极,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为O2+2CO2+4e-═2CO32-,故B正确;
C.石墨电极上析出的气体为氢气,生成44.8L氢气转移电子的物质的量=
×2=4mol,根据转移电子相等得,消耗氧气的物质的量=
=1mol,故C错误;
D.水是弱电解质,其导电能力较小,为了增强溶液的导电能力而加入强电解质,故D正确;
故选C.
B.通入空气的电极为正极,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为O2+2CO2+4e-═2CO32-,故B正确;
C.石墨电极上析出的气体为氢气,生成44.8L氢气转移电子的物质的量=
| 44.8L |
| 22.4L/mol |
| 4mol |
| 4 |
D.水是弱电解质,其导电能力较小,为了增强溶液的导电能力而加入强电解质,故D正确;
故选C.

练习册系列答案
相关题目