题目内容
【题目】为了测定某有机物A的结构,做如下实验:

①将4.4g该有机物完全燃烧,生成 0.2mol CO2和3.6g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③A的核磁共振氢谱如图2:
试回答下列问题:
(1)有机物A的相对分子质量是_____________
(2)有机物A的实验式是_____________
(3)有机物A的分子式是_____________
(4)红外光谱上发现A有﹣COOH和2个﹣CH3则有机物A的结构简式 ________________
【答案】 88 C2H4O C4H8O2 (CH3)2CHCOOH;
【解析】(1)由已知②用质谱仪测定其相对分子质量,得如图1所示的质谱图,根据该有机物的质谱图可知,其相对分子质量为88。
(2)由已知①将4.4g该有机物完全燃烧,生成0.2molCO2和3.6g水,4.4g该有机物的物质的量为:4.4g÷88gmol-1=0.05mol,3.6g水的物质的量为:3.6g÷18gmol-1=0.2mol;4.4g该有机物中含C、H的质量共:12gmol-1×0.2mol+1gmol-1×0.2mol×2=2.8g,根据质量守恒定律,4.4g该有机物分子中还含有1.6g(即0.1mol)氧原子,所以该有机物分子中C、H、O原子个数比为:0.2:0.2×2:0.1=2:4:1,故实验式为:C2H4O。
(3)因为该有机物实验式为C2H4O,所以可设分子式为(C2H4O)n,根据相对分子质量是88可得:(12×2+1×4+16)n=88,解得n=2,所以分子式为:C4H8O2。
(4)红外光谱上发现A有-COOH和2个-CH3,结合该有机物分子式C4H8O2可知,其结构简式为:(CH3)2CHCOOH。

【题目】一定条件下将质量m g的有机物在氧气中完全燃烧,燃烧后全部产物缓慢通过足量过氧化钠,充分反
应后过氧化钠固体增重n g,关于下列情况说法正确的是
有机物 | n | |
A | CH4 | 2m |
B | HCHO | 3m/2 |
C | CH3OH和CH3COOH的混合物 | 2m/3 |
D | C2H5OH和CH3COOC2H5的混合物 | m |
A. A B. B C. C D. D
【题目】分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛。环己醇中加入浓硫酸后适当加热脱水 是 合 成 环 己烯的常用 方法 , 实验 室合成坏己烯的反应和 实验 装 置如图:
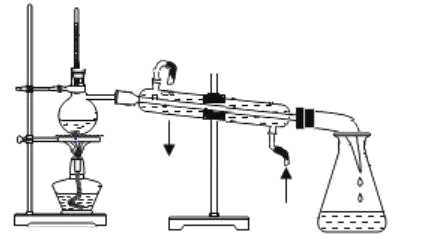
可能用到的有关数据如下:
相对分子质量 | 密度 / ( gcm― 3 ) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环 己烯 | 82 | 0.8102 | 83 | 难溶于水 |
I.合成反应:
在 a 中 加入 20g 环己醇 和 2 小片碎瓷片,冷却搅动下慢慢加入 1 ml 浓 硫 酸 , b 中 通入冷 却水后,开始缓慢加热 a ,控制馏出物的温度不超过 90℃.
Ⅱ. 分离提纯 :
反应粗产物倒入分液漏斗 中 分别用少量 5% 碳酸钠溶液和水洗涤, 分离 后加入无水氯化 钙颗粒,静置一段时间后弃去氯化钙,最终通过 蒸馏 得到纯净 环 己烯 10g . 回答下列问题:
(1)加入碎瓷片的作用是 _____; 如 果 加 热 一 段 时 间 后 发 现 忘 记 加 瓷 片 , 应 该 采 取 的正确操作是 _____(填 字母代号 ).
A .立即补加 B .冷却后补加
C .不需补加 D .重新配料
(2)在本 实验分离 过程中 ,产物应该从分液漏斗的 _______(填 “上口倒出 ”或 “下口倒 出 ”). 理由是 _____。
(3)分离提纯过 程 中 加入无水氯化钙的目的是 _____.
(4)在 环 己烯粗产物 蒸馏 过程 中 ,不可能用到的仪器有 ________(填 字母代号 ).
A . 蒸馏 烧瓶 B .温度计 C .分液漏斗
D .牛角管 E .锥形瓶.