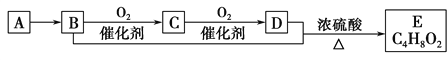
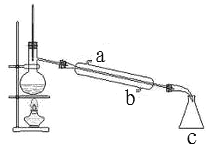
��Ŀ����
����Ŀ��������(GaN)����Ϊ�������뵼���������Ӧ���Ѿ�ȡ����ͻ���ԵĽ�չ��
��֪����i�������������ȶ�������ˮ���ᷴӦ��ֻ�ڼ���ʱ����Ũ����
��ii��NiCl2 ��Һ�ڼ���ʱ����ת��ΪNi(OH)2����ֽ�ΪNiO��
��iii���Ʊ������صķ�ӦΪ��2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
ijѧУ��ѧ��ȤС��ʵ�����Ʊ������������ʵ��װ����ͼ��ʾ��
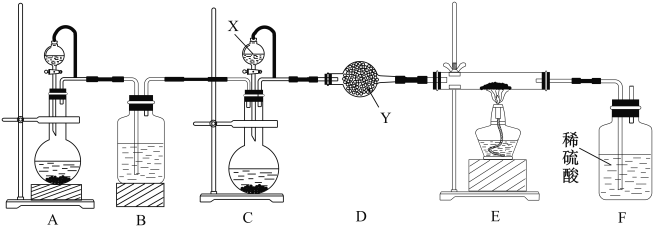
���ʵ�鲽��������
���μӼ���NiCl2 ��Һ��ʪ�����ط�ĩ�����ڷ�Ӧ���ڡ�
����ͨ��һ��ʱ����H2���ټ��ȡ�
��ֹͣͨ��������ͨ�백������������һ��ʱ�䡣
��ֹͣ����������ͨ�백��,ֱ����ȴ��
������Ӧ���ڵĹ���ת�Ƶ�ʢ��������ձ��У���ַ�Ӧ���ˡ�ϴ�ӡ����
��1������X�е��Լ���___________������Y��������__________________��
��2��ָ������װ���д���һ�����ԵĴ�����________________________��
��3����������ѡ��NiCl2 ��Һ����ѡ����������ԭ����____________________��
a.����Ӵ�������ӿ컯ѧ��Ӧ����
bʹ���ܾ��ȸ������ط۵ı��棬��ߴ�Ч��
c.Ϊ���ܸ����γ�ԭ��أ��ӿ췴Ӧ����
��4�����������Ʊ������أ����жϸ÷�Ӧ�ӽ����ʱ�۲쵽��������____________________��
��5����д���������м����Ʒ�����ع���ϴ�Ӹɾ��IJ���________________________��
��6����Ԫ������ͬ�壬�������������ƣ���д��������������NaOH��Һ�����ӷ���ʽ��______________________��
���𰸡� Ũ��ˮ ���θ���� װ��F�л�������� a b װ��F�м������ٲ������� ȡ����һ��ϴ��Һ���Թ��У��μ�AgNO3��Һ�����ް�ɫ��������֤����Ʒ�����ع�����ϴ�Ӹɾ� GaN��OH����H2O ![]() GaO
GaO![]() ��NH3��
��NH3��
����������1������������Ϣ��֪��װ��A��ȡ������װ��C��ȡ����������Ҫ��������Һ������������ư�����������X�е��Լ���Ũ��ˮ������Y�����������θ���ܣ���2��������İ�������װ��F��Ũ���ᷴӦ��װ��F�л������������3���������ѡ��NiCl2��Һ��NiCl2��Һ�ڼ���ʱ����ת��ΪNi(OH)2����ֽ�ΪNiO������Ӵ�������ӿ컯ѧ��Ӧ���ʣ�ʹ���ܾ��ȸ������ط۵ı��棬��ߴ�Ч�ʣ���ѡa b����4�����������Ʊ������أ���ӦΪ��2Ga+2NH3![]() 2GaN+3H2��������������ˮ������������ˮ�����жϸ÷�Ӧ�ӽ����ʱ�۲쵽��������װ��F�м������ٲ������ݣ���5���������м����Ʒ�����ع���ϴ�Ӹɾ��IJ�����ȡ����һ��ϴ��Һ���Թ��У��μ�AgNO3��Һ�����ް�ɫ��������֤����Ʒ�����ع�����ϴ�Ӹɾ�����6����Ԫ������ͬ�壬�������������ƣ���������������Һ��Ӧ�����ӷ���ʽΪ��2Al��2OH����2H2O
2GaN+3H2��������������ˮ������������ˮ�����жϸ÷�Ӧ�ӽ����ʱ�۲쵽��������װ��F�м������ٲ������ݣ���5���������м����Ʒ�����ع���ϴ�Ӹɾ��IJ�����ȡ����һ��ϴ��Һ���Թ��У��μ�AgNO3��Һ�����ް�ɫ��������֤����Ʒ�����ع�����ϴ�Ӹɾ�����6����Ԫ������ͬ�壬�������������ƣ���������������Һ��Ӧ�����ӷ���ʽΪ��2Al��2OH����2H2O ![]() 2AlO
2AlO![]() ��3H2��������������NaOH��Һ�����ӷ���ʽΪ��GaN��OH����H2O
��3H2��������������NaOH��Һ�����ӷ���ʽΪ��GaN��OH����H2O ![]() GaO
GaO![]() ��NH3����
��NH3����

 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�