题目内容
下图是硫酸试剂瓶标签上的内容。
| 硫酸:化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g·cm-3 质量分数:98% |
(2)实验室用该硫酸配制240mL 0.46mol/L的稀硫酸,则
①有以下仪器: A.烧杯 B.100mL量筒 C.250mL容量瓶 D.500mL容量瓶 E.玻璃棒 F.托盘天平(带砝码)G.10mL量筒H.胶头滴管,配制时,必须使用的仪器有 (填代号).
②需要该硫酸的体积为 mL.
③下图为配制过程中的几个关键步骤和操作:将上述实验步骤A—F按实验过程
先后次序排列 。
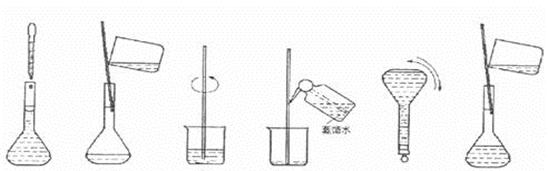
|
④该同学实际配制得到的浓度为0.45mol/L,可能的原因是
A.量取浓H2SO4时仰视刻度
B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶
D.定容时仰视刻度
(1)18.4mol/L (2分,单位没有给1分);
(2)①ACEGH;(2分,多选不给分)②6.25或6.3ml(2分);
③CBDFAE(2分,有次序错就全错)④C、D(2分,漏选扣1分)
解析试题分析:(1)由溶质的质量分数求物质的量浓度时可依据公式c=1000ρω/M来计算,代入数据可求得,c=18.4mol·L-1。
(2)①配制240mL 0.46mol/L的稀硫酸,需要使用250ml容量瓶,量取浓硫酸使用10ml量筒,在烧杯中溶解,溶解和移液用玻璃棒,定容用胶头滴管,故选用ACEGH。
②由稀释前后溶质的物质的量不变可知,18.4mol·L-1×V=4.6mol·L-1×0.25 L,则V=0.063 L=6.3ml。
③按照溶解、转移、洗涤、定容、摇匀的顺序进行排列,故正确顺序为:CBDFAE。
④实际配制得到的浓度为0.45mol/L,浓度变小,A、量取浓H2SO4时仰视刻度,造成H2SO4量取的体积增大,配制溶液的浓度增大;B、容量瓶未干燥,不影响浓度;C、没有将洗涤液转入容量瓶,造成溶质减小,浓度偏小;D、定容时仰视刻度,造成溶液体积变大,配制的溶液浓度减小。
考点:本题考查配制一定物质的量浓度的溶液仪器的选择、实验步骤、误差分析及相关计算。

镁、铝、铁及其化合物在生产和生活中有广泛的应用。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)= 。
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2→2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为 。
(3)现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):纵坐标中A点的数值是 。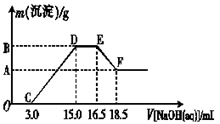
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为 (最简单的整数比)。
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
则该硫酸溶液的物质的量浓度为 。
③若在上述实验Ⅱ中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为 g (保留3位小数)
下列有关物质应用的说法错误的是
| A.CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒物质,现已被禁用 |
| B.工厂中常用的静电除尘装置是根据胶体带电这个性质而设计的。 |
| C.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 |
| D.为了延长果实或花朵的成熟期,可用浸泡过高锰酸钾溶液的硅土吸收水果或花朵产生的乙烯。 |
从分类角度,下列说法正确的是
| A.水玻璃与硅胶均属于酸 |
| B.漂白液与漂粉精的主要成分均为钠盐 |
| C.NO2、SO3均属于酸性氧化物 |
| D.醋酸、一水合氨均属于弱电解质 |
全部属于纯净物的组合是( )
| A.福尔马林、白酒、食醋 | B.汽油、油脂、酚醛树脂 |
| C.石炭酸、盐酸、冰醋酸 | D.甘油、乙醇钠、氯仿 |
分类是化学研究的重要方法之一,下列有关说法中,正确的是
A.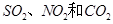 都属于酸性氧化物 都属于酸性氧化物 |
| B.甲烷和和一氯甲烷都属于烷烃 |
| C.HC1O是弱电解质,NaClO却属于强电解质 |
| D.在水溶液中能电离出H+的化合物都属于酸 |

