题目内容
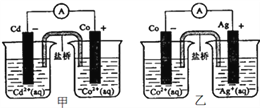
【题目】下图甲和乙是双液原电池装置,据图判断下列说法错误的是( )
A. 盐桥的作用是形成闭合回路,并使两边溶液保持电中性
B. 甲图,电池反应的离子方程式为: Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq)
C. 乙图,当有1mol电子通过外电路时,正极有108gAg析出
D. 反应: 2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)能够发生
【答案】D
【解析】A.原电池放电时,盐桥中的阴阳离子定向移动而构成闭合回路,且使两溶液中电荷相等,所以盐桥的作用是形成闭合回路,并使两边溶液保持电中性,选项A正确;B.根据原电池甲可知,Cd为负极,失电子,Co2+得电子,所以其电池反应离子方程式为Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq),金属活动性Cd>Co,选项B正确;C.根据Co(s)+2Ag +(aq)=2Ag(s)+Co2+(aq)知,当有lmol电子通过外电路时,正极有108g Ag析出,选项C正确;D.根据原电池乙可知,Co失电子,Ag + 得电子,所以Co(s)+2Ag +(aq)=2Ag(s)+Co2+(aq),金属活动性Co>Ag,则有金属活动性:Cd>Co>Ag,因此2Ag(s)+ Cd2+(aq) = Cd(s) +2Ag+(aq)反应不能发生,选项D错误。答案选D。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
【题目】根据下表中所列键能数据,判断下列分子中,最不稳定的分子是( )
化学键 | H—H | H—Cl | H—I | Cl—Cl | Br—Br |
键能/kJ/mol | 436 | 431 | 299 | 247 | 193 |
A.HClB.HBrC.H2D.Br2