题目内容
3.短周期元素X、Y、Z、W原子序数依次增大.X的质子数与电子层数相同,Y、Z同周期且相邻,Z的最外层电子数是其内层电子数的3倍,元素W在地壳中的含量仅次于氧.下列说法正确的是( )| A. | 原子半径:r(W)>r(Y)>r(Z)>r(X) | |
| B. | X、Y、Z三种元素形成的化合物中只有共价键 | |
| C. | 最高价氧化物对应水化物的酸性:W>Y | |
| D. | 气态简单氢化物的热稳定性:Y>Z |
分析 短周期元素X、Y、Z、W原子序数依次增大,X的质子数与电子层数相同,则X为H元素;Z的最外层电子数是其内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故Z为O元素;Y、Z同周期且相邻,则Y为N元素;元素W在地壳中的含量仅次于氧,则W为Si,据此解答.
解答 解:短周期元素X、Y、Z、W原子序数依次增大,X的质子数与电子层数相同,则X为H元素;Z的最外层电子数是其内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故Z为O元素;Y、Z同周期且相邻,则Y为N元素;元素W在地壳中的含量仅次于氧,则W为Si.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,所有元素中H原子半径最小,故原子半径:r(Si)>r(N)>r(O)>r(H),故A正确;
B.X、Y、Z三种元素形成的化合物NH4NO3中含有离子键、共价键,故B错误;
C.非金属性Y(N)<Z(O),故氢化物稳定性:NH3<H2O,故D错误;
D.非金属性Y(N)>W(Si),故酸性:硝酸>硅酸,故C错误,
故选A.
点评 本题考查原子结构与元素周期律,推断元素是解题关键,侧重对元素周期律的考查,难度不大.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
11.X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是( )
| A. | 一定是离子化合物 | |
| B. | R 一定是共价化合物 | |
| C. | R可能是液态物质,也可能是固态物质 | |
| D. | R可能是共价化合物,也可能是离子化合物 |
12.一定条件下,将A、B、C三种气体各1mol通入一个密闭容器中发生反应,2A+B?2C,达到化学平衡时,B的物质的量可能是( )
| A. | 1.5mol | B. | 1mol | C. | 0mol | D. | 0.5mol |
11.一定量的CuS投入足量的HNO3中,收集到标准状况下的气体VL,向反应后的溶液中加入足量的NaOH,产生蓝色沉淀,经过滤、洗涤、灼烧,得到CuO12g,若上述气体为NO和NO2的混合物,且体积比为1:1,则V为( )
| A. | 9.0L | B. | 13.44L | C. | 15.7L | D. | 16.8L |
8.关于如图装置的下列叙述中不正确的是( )
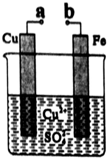

| A. | 无论a和b是否连接,该装置的反应原理相同 | |
| B. | a和b分别连接直流电源正、负极可以实现铁上镀铜 | |
| C. | a和b不连接时反应速率比a和b用导线连接时的速率慢 | |
| D. | 在a、b之间连接一小灯泡,改变Cu2+的浓度不会影响灯泡亮度 |
15.下列说法不正确的是( )
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 蛋白质溶液遇醋酸铅溶液发生盐析 | |
| C. | 氨基酸、二肽、蛋白质均既能跟强酸反应又能跟强碱反应 | |
| D. | 乙二醇、甲醛、α-羟基丙酸(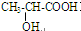 )都可发生缩聚反应 )都可发生缩聚反应 |
12.利用图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 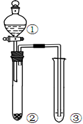 |
| A | 稀硫酸 | Na2CO3 | C6H5ONa | 酸性:H2CO3>C6H5OH | |
| B | 液溴和苯 | 铁屑 | AgNO3溶液 | 液溴和苯发生取代反应 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐可以生成白色沉淀 | |
| D | 浓盐酸 | KMnO4 | FeBr2溶液 | 氧化性:Cl2>Br2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
13.硒(Se)与硫在元素周期表中位于同一主族.下列说法不正确的是( )
| A. | 原子半径:Se>S | B. | 沸点:H2S>H2Se | ||
| C. | 稳定性:H2S>H2Se | D. | 酸性:H2SO4>H2SeO4 |
 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.