题目内容
【题目】下列实验操作能达到目的的是( )
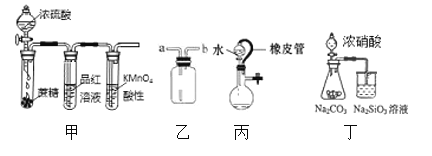
A. 用甲装置验证浓H2SO4的脱水性、强氧化性
B. 用乙装置收集NO气体
C. 装置丙中水能持续流下,说明装置气密性不良好
D. 用丁装置比较N、C、Si非金属性的强弱
【答案】A
【解析】
A.浓硫酸和蔗糖发生氧化还原反应生成二氧化碳、二氧化硫、水等物质,该反应中浓硫酸将蔗糖氧化,二氧化硫能使品红溶液褪色而体现漂白性,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以体现二氧化硫还原性,所以该实验验证浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性,故A正确;
B.NO能和空气中氧气反应,收集NO也不能用排空气法收集,故B错误;
C.分液漏斗和蒸馏烧瓶用橡皮管连接,两个容器中压强相等,则分液漏斗中的水能够顺利流向,所以该操作方法无法判断装置气密性,故C错误;
D.浓硝酸具有挥发性导致二氧化碳中含有HNO3,而影响二氧化碳和硅酸钠溶液的反应,无法证明碳酸的酸性比硅酸强,故D错误;
故答案为A。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
②CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
③CH3OH(g)![]() CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
回答下列问题:
(1)已知反应②中相关化学键键能数据如下:
化学键 | H-H | C=O | C≡O | H-O |
E/kJ·mol-1 | 436 | 803 | 1076 | 465 |
由此计算ΔH2=____kJ·mol-1。已知ΔH3=+99kJ·mol-1,则ΔH1=____kJ·mol-1。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。

①温度为470K时,图中P点____(填“是”或“不是”)处于平衡状态。在490K之前,甲醇产率随温度升高而增大,490K之后,甲醇产率随温度升高而减小的原因分别是____。
②一定能提高甲醇产率的措施是____。
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。

①490K时,根据曲线a、c判断合成甲醇的反应机理是____(填“I”或“II”)。
Ⅰ.CO2![]() CO
CO![]() CH3OH II.CO
CH3OH II.CO![]() CO2
CO2![]() CH3OH+H2O
CH3OH+H2O
②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从热力学与动力学角度,并结合反应①、②分析原因____。
【题目】下表中是各组反应的反应物和反应温度,反应刚开始时,放出H2速率最快的是( )
编号 | 金属(粉末状) | 物质的量(mol) | 酸的浓度及体积 | 反应温度(℃) |
A | Al | 0.1 | 2mol.L-1盐酸10mL | 60 |
B | Fe | 0.1 | 1mol.L-1盐酸10mL | 50 |
C | Mg | 0.1 | 1mol.L-1盐酸10mL | 60 |
D | Mg | 0.1 | 1mol.L-1硫酸10mL | 60 |
A.AB.BC.CD.D


