题目内容
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:______。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是______反应。
(2)甲和乙两个水浴作用不相同,甲的作用是_________;乙的作用是:________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是____。集气瓶中收集到的气体的主要成分是______。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。
【答案】2Cu+O2![]() 2CuO 、CH3CH2OH+CuO
2CuO 、CH3CH2OH+CuO![]() CH3CHO+H2O+Cu 放热 加热 冷却 乙醛、乙醇、水 、氮气 乙酸
CH3CHO+H2O+Cu 放热 加热 冷却 乙醛、乙醇、水 、氮气 乙酸
【解析】
(1)铜网出现黑色,发生的反应为:2Cu+O2![]() 2CuO,黑色变为红色,发生的反应为:CH3CH2COH+CuO
2CuO,黑色变为红色,发生的反应为:CH3CH2COH+CuO![]() CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是放热反应;
CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是放热反应;
(2)甲装置的作用是用热水浴加热使乙醇挥发与空气中的氧气混合,有利于下一步反应;乙处使用的为冷水浴,降低温度,使生成的乙醛冷凝成为液体;即前者的答案为加热,后者为冷却;
(3)乙醇催化氧化生成乙醛和水,有一部分乙醇没有参加反应,因此干燥试管a中能收集到的物质的是水、乙醇和乙醛;空气中主要成分是N2和O2,氧气参与反应,即最后收集到的气体主要为氮气;
(4)紫色石蕊遇酸变红,说明部分乙醛被氧化成了乙酸,即液体中还含有的物质是乙酸。

【题目】卤素的单质和化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。回答下列问题:
(1)溴原子的价层电子排布图为_______。根据下表提供的第一电离能数据,判断最有可能生成较稳定的单核阳离子的卤素原子是________(填元素符号)。
氟 | 氯 | 溴 | 碘 | |
第一电离能/ (kJ·mol-1) | 1 681 | 1 251 | 1 140 | 1 008 |
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合[(HF)2]形式存在,使氟化氢分子缔合的相互作用是____________。碘在水中溶解度小,但在碘化钾溶液中明显增大,这是由于发生反应:I-+I2=I3-,CsICl2与KI3类似,受热易分解,倾向于生成晶格能更大的物质,试写出CsICl2受热分解的化学方程式:_________________________________。
(3)ClO2-中心氯原子的杂化轨道类型为________,与ClO2-具有相同立体构型和键合形式的物质的化学式为____________(写出一个即可)。
(4)如图甲为碘晶体晶胞结构,平均每个晶胞中有________个碘原子,碘晶体中碘分子的配位数为____________。


(5)已知NA为阿伏加德罗常数,CaF2晶体密度为ρ g·cm-3,其晶胞如图乙所示,两个最近Ca2+核间距离为a nm,则CaF2的相对分子质量可以表示为____________。
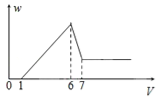
【题目】向物质Y中逐渐加入(或通入)X溶液,生成沉淀的量与加入X的物质的量关系如图所示,下表中符合图示情况的是
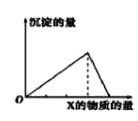
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D